
Wetenschap
Hoe de polariteit van water het leven vormgeeft:van oplosbaarheid tot plantentransport
Door Chris Deziel Bijgewerkt op 24 maart 2022
thomasmales/iStock/GettyImages
Het watermolecuul is elektrisch neutraal, maar de asymmetrische opstelling van de waterstofatomen op het zuurstofatoom geeft het een netto positieve lading aan de ene kant en een negatieve lading aan de andere kant. Tot de belangrijke gevolgen voor levende organismen behoren het vermogen van water om een verscheidenheid aan stoffen op te lossen, meer dan welke andere vloeistof dan ook, en de sterke oppervlaktespanning ervan, waardoor het druppels kan vormen en door kleine wortels, stengels en haarvaten kan reizen. Water is de enige substantie die bestaat als gas, vloeistof en vaste stof bij temperaturen die op aarde voorkomen, en vanwege de polariteit van het watermolecuul is de vaste toestand minder dicht dan de vloeibare toestand. Als gevolg hiervan drijft ijs, en dit heeft diepgaande gevolgen voor het leven overal op de planeet.
Waterstofbinding
Waterstofbinding
Een gemakkelijke manier om de polaire aard van een watermolecuul te waarderen, is door het te visualiseren als het hoofd van Mickey Mouse. De waterstofatomen zitten bovenop het zuurstofmolecuul, op vrijwel dezelfde manier als de oren op Mickey's hoofd. Deze vervormde tetraëdrische opstelling komt tot stand vanwege de manier waarop elektronen tussen de atomen worden gedeeld. De waterstofatomen vormen een hoek van 104,5 graden, waardoor elk molecuul de kenmerken heeft van een elektrische dipool of een magneet.
De positieve (waterstof) kant van elk watermolecuul wordt aangetrokken door de negatieve (zuurstof) kant van omringende moleculen in een proces dat waterstofbinding wordt genoemd. Elke waterstofbrug duurt slechts een fractie van een seconde en is lang niet sterk genoeg om de covalente bindingen tussen de atomen te verbreken, maar het geeft water een abnormaal karakter in vergelijking met andere vloeistoffen, zoals alcohol. Drie afwijkingen zijn vooral belangrijk voor levende organismen.
Het oplosmiddel van het leven
Het oplosmiddel van het leven
Vanwege zijn polaire aard kan water zoveel stoffen oplossen dat wetenschappers het soms een universeel oplosmiddel noemen. Organismen nemen veel essentiële voedingsstoffen op, waaronder koolstof, stikstof, fosfor, kalium, calcium, magnesium en zwavel uit water. Bovendien, wanneer water een ionische vaste stof, zoals natriumchloride, oplost, drijven de ionen vrij in de oplossing en veranderen deze in een elektrolyt. Elektrolyten geleiden de elektrische signalen die nodig zijn om neurale signalen over te brengen, evenals signalen die andere biofysische processen reguleren. Water is ook het medium waarmee organismen de afvalproducten van de stofwisseling elimineren.
De bindende kracht van voeding
De bindende kracht van voeding
Door de elektrostatische aantrekking van watermoleculen tot elkaar ontstaat het fenomeen oppervlaktespanning, waarbij het oppervlak van vloeibaar water een barrière vormt waarop bepaalde insecten daadwerkelijk kunnen lopen. De oppervlaktespanning zorgt ervoor dat water zich tot druppeltjes vormt, en wanneer de ene druppel de andere nadert, trekken ze elkaar aan en vormen ze één druppel.
Vanwege deze aantrekkingskracht kan water als een gestage stroom in kleine haarvaten worden gezogen. Hierdoor kunnen planten via hun wortels vocht uit de grond halen, en kunnen hoge bomen voeding krijgen door sap door hun poriën te zuigen. De aantrekking van watermoleculen tot elkaar zorgt er ook voor dat vloeistoffen door de lichamen van dieren blijven circuleren.
De anomalie van drijvend ijs
De anomalie van drijvend ijs
Als het ijs niet zou drijven, zou de wereld er anders uitzien en waarschijnlijk geen leven kunnen ondersteunen. Oceanen en meren kunnen van onderaf bevriezen en in een vaste massa veranderen zodra de temperatuur koud wordt. In plaats daarvan vormen waterlichamen in de winter een ijslaag; het wateroppervlak bevriest wanneer het wordt blootgesteld aan de koudere luchttemperaturen erboven, maar het ijs blijft bovenop de rest van het water omdat ijs minder dicht is dan water. Hierdoor kunnen vissen en andere zeedieren overleven bij koud weer en voedsel leveren aan landdieren.
Met uitzondering van water wordt elke andere verbinding in vaste toestand dichter dan in vloeibare toestand. Het unieke gedrag van water is een direct gevolg van de polariteit van het watermolecuul. Terwijl de moleculen zich in de vaste toestand nestelen, worden ze door waterstofbruggen in een roosterstructuur gedwongen die meer ruimte tussen hen biedt dan in de vloeibare toestand.
 Fernanda verzwakt tot tropische storm
Fernanda verzwakt tot tropische storm Is een ecosysteem of herbivoren voedingsstoffen en mineralen het belangrijkst in de voedselketen?
Is een ecosysteem of herbivoren voedingsstoffen en mineralen het belangrijkst in de voedselketen?  Snakes Found in Northern Illinois
Snakes Found in Northern Illinois  Nieuw internationaal initiatief benadrukt de noodzaak van wereldwijde actie tegen luchtvervuiling, aangezien de gevolgen voor de gezondheid groot blijven
Nieuw internationaal initiatief benadrukt de noodzaak van wereldwijde actie tegen luchtvervuiling, aangezien de gevolgen voor de gezondheid groot blijven Oorzaak, omvang vastgesteld voor dodelijke winterafvalstroom in Uttarakhand, India
Oorzaak, omvang vastgesteld voor dodelijke winterafvalstroom in Uttarakhand, India
Hoofdlijnen
- Waarom je haar en nagels niet groeien na de dood:de mythe ontkrachten
- Is prokaryotisch gevonden in dieren- of plantencellen?
- Is een koninkrijk schimmels uniclellulair of multicellulair?
- Zijn mensen het slimste dier?
- Tabaksplanten als levensredders
- Wat doen endospores?
- Dit is wat de wetenschap zegt over het gevoel van dieren
- Wat is het macro -ecosysteem?
- Wat vormt de celwanden van schimmelcellen?
- Wetenschappers maken sensoren met vallen voor vrije radicalen
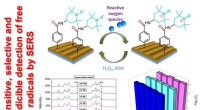
- Ons water reinigen met baanbrekende bio-geïnspireerde chemie
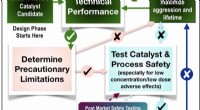
- Onderzoekers rapporteren nieuwe methode voor het karakteriseren van materialen die uiteindelijk kunnen helpen energie op te slaan

- Nieuw onderzoek laat zien hoe geclusterde deeltjes de elasticiteit van sommige gels bepalen

- Menselijke gevaren belemmeren onderzoek naar gif van vampiervleermuizen

 Wat is de overgroei van vezelig weefsel dat gewoonlijk op de plaats van een skar wordt geproduceerd?
Wat is de overgroei van vezelig weefsel dat gewoonlijk op de plaats van een skar wordt geproduceerd?  Afbeelding:Voorgrondasteroïde die de Krabnevel passeert
Afbeelding:Voorgrondasteroïde die de Krabnevel passeert Waarom botst het elektron in waterstof niet met het proton?
Waarom botst het elektron in waterstof niet met het proton?  Zijn herfstbladeren kleurrijker na een natte of droge zomer?
Zijn herfstbladeren kleurrijker na een natte of droge zomer?  Stamcelvaccins:een veelbelovende nieuwe grens in de kankertherapie
Stamcelvaccins:een veelbelovende nieuwe grens in de kankertherapie  Geen 'wiskundemens'? Misschien ben je beter in het leren coderen dan je denkt
Geen 'wiskundemens'? Misschien ben je beter in het leren coderen dan je denkt  De Wordle-rage:waarom houden we van puzzels en zijn ze goed voor onze hersenen?
De Wordle-rage:waarom houden we van puzzels en zijn ze goed voor onze hersenen?  Hoe wordt het DNA opgeroepen?
Hoe wordt het DNA opgeroepen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

