
Wetenschap
Lewis-puntstructuren beheersen:valentie-elektronen voor elk element tellen
Door Sean Lancaster
Bijgewerkt op 30 augustus 2022
Lewis-puntdiagrammen bieden een beknopte visuele weergave van de valentie-elektronenverdeling in covalente moleculen, waardoor scheikundigen snel bindingspatronen kunnen beoordelen. Nauwkeurige constructie van een Lewis-structuur vereist kennis van de valentie-elektronen van het atoom. Het periodiek systeem rangschikt elementen op basis van chemische gelijkenis; de lay-out weerspiegelt het aantal valentie-elektronen, waarbij het s-blok (kolommen 1–2) en p-blok (kolommen 13–18) de valentie-orbitalen weergeven die betrokken zijn bij covalente binding.
Stap 1
Zoek het element op het periodiek systeem. De positie ervan onthult het aantal valentie-elektronen, die de basis vormen van elk Lewis-puntdiagram.
Stap 2
Schrijf het chemische symbool van het element. De meeste atomen kunnen maximaal acht valentie-elektronen bevatten; waterstof en helium bevatten er twee. Overgangsmetalen kunnen maximaal achttien elektronen accepteren, maar wijken vaak af van de octetregel en vormen complexe coördinatieverbindingen.
Stap 3
Schik de valentie-orbitalen rond het symbool. Voor enkelvoudig gebonden atomen plaatst u de orbitalen symmetrisch aan weerszijden van het symbool. Dubbele bindingen worden weergegeven door twee elektronen in een van de drie orbitalen met een tussenruimte van 120°; Bij drievoudige bindingen zijn drie elektronen betrokken in een lineaire opstelling. Elke orbitaal kan maximaal twee elektronen bevatten.
Stap 4
Tel het groepsnummer van het element. In het periodiek systeem geven de eerste twee (s-blok) en laatste zes (p-blok) kolommen het aantal valentie-elektronen aan. Overgangsmetalen (d-blok) bevatten ook valentie-elektronen, hoewel hun bindingsgedrag complexer is.
Stap 5
Verdeel de valentie-elektronen. Wijs één elektron per orbitaal toe totdat alle orbitalen afzonderlijk bezet zijn, en voeg indien nodig het tweede elektron toe aan dezelfde orbitaal. Bij dubbele of drievoudige bindingen bevinden de gedeelde elektronen zich tussen de twee gebonden atomen.
 De plasticafvalcrisis is een kans voor de VS om thuis serieus te gaan recyclen
De plasticafvalcrisis is een kans voor de VS om thuis serieus te gaan recyclen Langer modderseizoen, geen sneeuw zou de noordoostelijke rivieren kunnen veranderen tegen het jaar 2100
Langer modderseizoen, geen sneeuw zou de noordoostelijke rivieren kunnen veranderen tegen het jaar 2100 De langzame aardbevingen die we niet kunnen voelen, kunnen helpen beschermen tegen de verwoestende aardbevingen
De langzame aardbevingen die we niet kunnen voelen, kunnen helpen beschermen tegen de verwoestende aardbevingen Plantennomenclatuur:hoe namen het uiterlijk van planten onthullen
Plantennomenclatuur:hoe namen het uiterlijk van planten onthullen  Zou het opruimen van stranden Amerikanen beter af kunnen maken?
Zou het opruimen van stranden Amerikanen beter af kunnen maken?
Hoofdlijnen
- Welk doel dienen verminderde mitochondriën?
- Opslagkamers binnen een cel heten?
- Welke cel helpt de plant de vorm te behouden?
- Produceert het lichaam niet -essentiële aminozuren?
- Wat is de wetenschap van het classificeren van organismen volgens hun evolutionaire relaties?
- Mensen en gorilla's hebben één ander aminozuur in hun hemoglobine -sequentie. Wat zegt dit over de evolutie van deze twee soorten?
- Welke eiwitten en andere materialen van het ene deel van de cel naar het andere?
- Wat onderscheidt de drie domeinen in het leven van het leven van elkaar?
- Wat betekent cardiobiologie?
- Kooldioxidemineralisatie in geologisch veel voorkomende gesteenten voor koolstofopslag

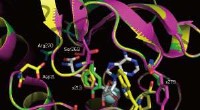
- Gerichte evolutie om enzymen te ontwerpen die beeldvormende middelen maken voor medische diagnose
- Hoe temperatuur de diffusie versnelt:inzichten voor chemici

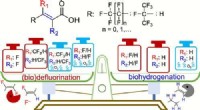
- Onder anaërobe omstandigheden kunnen gewone microbiële gemeenschappen de ultrasterke koolstof-fluorbinding verbreken
- De fundamentele chemie achter elektrokatalytische watersplitsing

 Wat gebeurt er als een planeet dichter bij de zon komt?
Wat gebeurt er als een planeet dichter bij de zon komt?  Hoe kunt u een object magnetiseren?
Hoe kunt u een object magnetiseren?  Nieuwe techniek voor het maken van NV-gedoteerde nanodiamanten kan een stimulans zijn voor kwantumcomputers
Nieuwe techniek voor het maken van NV-gedoteerde nanodiamanten kan een stimulans zijn voor kwantumcomputers Wetenschappers leggen het geluid van zonsopgang op Mars vast
Wetenschappers leggen het geluid van zonsopgang op Mars vast Waarom de ijsbedekking op Antarctica is toegenomen onder de gevolgen van klimaatverandering
Waarom de ijsbedekking op Antarctica is toegenomen onder de gevolgen van klimaatverandering  Wat is de snelheidswaarde op een sensorkiepte van 0,30 m 6,2 m op de meetlint?
Wat is de snelheidswaarde op een sensorkiepte van 0,30 m 6,2 m op de meetlint?  Hoeveel atomen bevat één formule-eenheid koper-11-sulfaat?
Hoeveel atomen bevat één formule-eenheid koper-11-sulfaat?  Rotsen die kristallen bevatten, vertonen welke textuur?
Rotsen die kristallen bevatten, vertonen welke textuur?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

