
Wetenschap
Gerichte evolutie om enzymen te ontwerpen die beeldvormende middelen maken voor medische diagnose
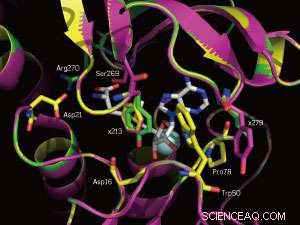
Een close-up van de SAM-bindingsplaatsen van het natieve enzym (geel) en twee mutanten (magenta en groen). De gemuteerde posities 213 en 279 zijn gelabeld. Krediet:WILEY-VCH Verlag GmbH &Co. KGaA, Weinheim
Organische moleculen die een fluoratoom bevatten, worden veel gebruikt in de materialen, agrochemische en farmaceutische industrie. Echter, het synthetiseren van de koolstof-fluorbinding maakt typisch gebruik van giftige metaalkatalysatoren en vereist watervrije omstandigheden en hoge temperaturen. Nu heeft een internationaal team een mildere, efficiëntere, op enzymen gebaseerde benadering om deze binding te creëren.
Deze enzymatische methode werkt in waterige omstandigheden en bij milde temperaturen en is ontwikkeld door een consortium met onderzoekers van A*STAR en andere instellingen. "Deze voorwaarden zijn echt zeer aantrekkelijk, " legt teamlid Yee Hwee Lim van het A*STAR Institute of Chemical and Engineering Sciences uit.
Het team gebruikte een van de zeer specifieke fluorinase-enzymen die in de natuur voorkomen:FlA1. Deze enzymen katalyseren de vorming van een koolstof-fluorbinding in S-adenosylmethionine (SAM) met behulp van anorganisch fluoride via een substitutiemechanisme.
Het enzym, terwijl het uitstekend is in het katalyseren van fluoreringsreacties met dit natuurlijke molecuul, werkte niet goed op niet-natuurlijke moleculen. Bovendien, pogingen om de structuren van de enzymen te wijzigen en, dus, functie was een strijd geweest - tot nu toe.
"We hebben voor het eerst aangetoond dat het fluorinase-enzym kan worden gemanipuleerd, en dat de techniek zijn enzymatische activiteit zelfs op niet-natuurlijke moleculen kan verbeteren, ' zegt Lim.
Het team gebruikte de gevestigde techniek die bekend staat als 'gerichte evolutie', die natuurlijke selectie nabootst om enzymen te ontwikkelen, zodat ze goed kunnen reageren met niet-natuurlijke moleculen.
"Gerichte evolutie is nooit met succes toegepast op dit enzym, tot nu, ", zegt Lim. "Dit is een moeilijk enzym om mee te werken en we stonden voor veel uitdagingen, waaronder problemen met productdegradatie."
Het team gebruikte de radiolabeling van 5'-chloor-5'-deoxyadenosine (5'-CIDA) om hun mogelijkheden te demonstreren. In deze tweestapsreactie, radioactief gemerkt 5'-CIDA wordt omgezet in SAM, en vervolgens gefluoreerd om 5'-fluor-5'-deoxyadenosine (5'-FDA) te vormen. Dit gelabelde 5'-FDA-product zou mogelijk kunnen worden gebruikt voor een medische diagnoseprocedure die bekend staat als positronemissietomografie (PET).
"We laten zien dat het drievoudig verbeteren van de activiteit van een enzym meer toepassingen kan openen, ", zegt Lim. "De inheemse enzymen zijn eerder gebruikt om PET-agentia te labelen, maar de reactietijden waren lang, soms uren. Met ons enzym konden we de reactie in 30 minuten doen, een redelijker tijdschema, aangezien de halfwaardetijd van Fluor-18 minder dan twee uur is."
Het team van Lim onderzoekt nu hoe het muteren van de structuur van het enzym de interactie met 5'-CIDA en SAM verandert. "Ik zou computationele biologen willen inschakelen om meer te begrijpen over de mutaties die we hebben gemaakt en hoe die correleren met onze reacties."
 Materiaalinformatica onthult nieuwe klasse van superharde legeringen
Materiaalinformatica onthult nieuwe klasse van superharde legeringen Onderzoeksteam reconstrueert motorvrachtcomplex voor ciliair transport
Onderzoeksteam reconstrueert motorvrachtcomplex voor ciliair transport Moleculaire motoren:Chemische carrousel draait in de kou
Moleculaire motoren:Chemische carrousel draait in de kou Vereenvoudigde methode maakt celvrije eiwitsynthese flexibeler en toegankelijker
Vereenvoudigde methode maakt celvrije eiwitsynthese flexibeler en toegankelijker Nieuwe kooldioxide-adsorberende kristallen voor biomedische materialen die afhankelijk zijn van vormgeheugeneffect
Nieuwe kooldioxide-adsorberende kristallen voor biomedische materialen die afhankelijk zijn van vormgeheugeneffect
 Studie:gletsjers in Azië worden geconfronteerd met enorme smelting door de opwarming van de aarde
Studie:gletsjers in Azië worden geconfronteerd met enorme smelting door de opwarming van de aarde Wat zijn de oorzaken van gevaarlijk afval?
Wat zijn de oorzaken van gevaarlijk afval?  Door het opdrogen van veengebieden neemt de vogeldiversiteit af
Door het opdrogen van veengebieden neemt de vogeldiversiteit af Natuurbrand in Californië bij Lake Tahoe bijna de helft onder controle
Natuurbrand in Californië bij Lake Tahoe bijna de helft onder controle Licht werpen op ijzerverrijking in de schemerzone van de oceanen
Licht werpen op ijzerverrijking in de schemerzone van de oceanen
Hoofdlijnen
- Waarom doden we?
- Een functionele genomics-database voor onderzoeken naar het microbioom van planten
- Leuke wetenschappelijke experimenten op cellen
- Regenboogpauwspinnen kunnen nieuwe optische technologieën inspireren
- Cellen puilen uit om door barrières te persen
- Sluwe kraaien weten wat er nodig is om een goed stuk gereedschap te maken
- Wat zijn de structurele delen van de lange botten in het lichaam?
- Wat zijn de zes soorten bindweefsel in de biologie?
Bindweefsel is een van de vier belangrijkste weefseltypen bij zoogdieren, de andere zijn zenuwweefsel, spierweefsel en epitheel of oppervlakteweefsel. Epitheliaal weefsel ligt op bindweefsel terwi
- Welke oorzaken smeren bij elektroforese?
- Studie onthult hoe zuurstofarm eiwit losjes bindt aan een mineraal
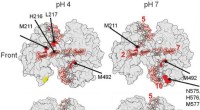
- Omkeerbare plakkerigheid in tandcement is iets om over te lachen
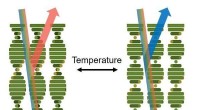
- Kleurveranderende coatings geactiveerd door temperatuurveranderingen
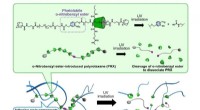
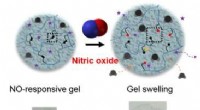
- Wetenschappers ontwikkelen potentieel therapeutische gel, die stikstofmonoxide detecteert, absorbeert overtollig vocht en geeft medicijnen af
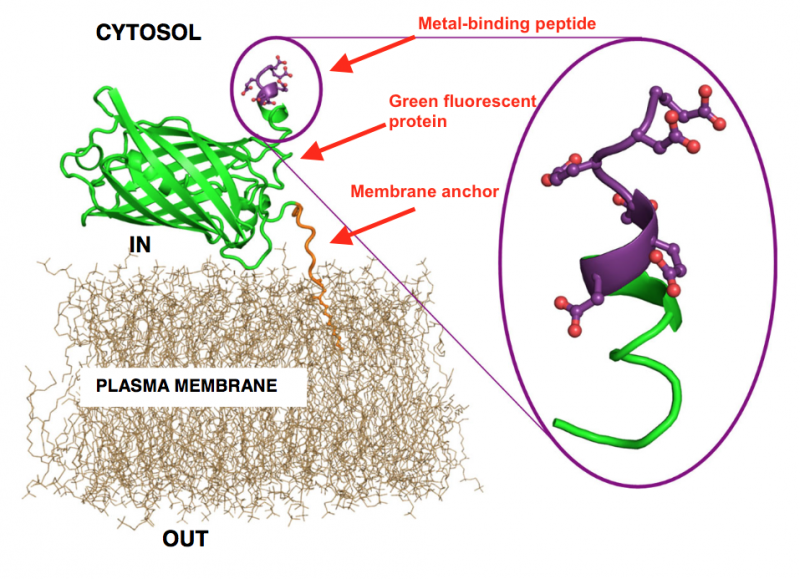
- Genetisch gemanipuleerde gist absorbeert vervuiling door zware metalen
 Hoe effectieve nucleaire lading te berekenen
Hoe effectieve nucleaire lading te berekenen Waarschuwing voor extreme hitte:wat de allereerste Met Office-waarschuwing betekent
Waarschuwing voor extreme hitte:wat de allereerste Met Office-waarschuwing betekent Voor de eerste keer, een ESA deep space-antenne bestuurde twee ruimtevaartuigen met één schotel
Voor de eerste keer, een ESA deep space-antenne bestuurde twee ruimtevaartuigen met één schotel Hoe zijn coniferen en varens anders?
Hoe zijn coniferen en varens anders?  United Technologies is van plan om 35, 000 mensen
United Technologies is van plan om 35, 000 mensen Ontwikkeling van een op nanofilm gebaseerde celkooitechnologie
Ontwikkeling van een op nanofilm gebaseerde celkooitechnologie Een levensechte deluminator voor het spotten van exoplaneten door gereflecteerd sterlicht
Een levensechte deluminator voor het spotten van exoplaneten door gereflecteerd sterlicht Wetenschappers halen waterstofgas uit olie en bitumen, potentiële vervuilingsvrije energie geven
Wetenschappers halen waterstofgas uit olie en bitumen, potentiële vervuilingsvrije energie geven
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

