
Wetenschap
Reactiviteit van niet-metalen:trends en verklaringen
* Elektronegativiteit: Niet-metalen hebben een hogere elektronegativiteit dan metalen. Dit betekent dat ze een sterkere aantrekkingskracht hebben op elektronen. Naarmate u zich door een periode beweegt, neemt de elektronegativiteit toe. Hierdoor is de kans groter dat niet-metalen elektronen opnemen en negatieve ionen vormen, wat leidt tot een grotere reactiviteit.
* Ionisatie-energie: Ionisatie-energie is de energie die nodig is om een elektron uit een atoom te verwijderen. Terwijl u zich door een periode beweegt, neemt de ionisatie-energie toe. Dit betekent dat het moeilijker wordt om elektronen uit de niet-metaalatomen te verwijderen, waardoor het minder waarschijnlijk is dat ze elektronen verliezen en eerder winnen, waardoor de reactiviteit verder toeneemt.
* Atomische grootte: De atoomgrootte neemt af naarmate je door een periode beweegt. Dit betekent dat de buitenste elektronen zich dichter bij de kern bevinden en een sterkere aantrekkingskracht ervaren. Dit draagt opnieuw bij aan de neiging van het niet-metaal om elektronen op te nemen, wat leidt tot een grotere reactiviteit.
Voorbeelden:
* Groep 17 (Halogenen): Fluor (F) is het meest reactieve niet-metaal in deze groep, gevolgd door chloor (Cl), broom (Br), jodium (I) en astatine (At). Deze trend wordt waargenomen omdat fluor de hoogste elektronegativiteit en de kleinste atoomgrootte binnen de groep heeft.
* Groep 16 (Chalcogenen): Zuurstof (O) is reactiever dan zwavel (S), dat reactiever is dan selenium (Se).
Uitzonderingen:
Hoewel de algemene trend voor niet-metalen een toename van de reactiviteit over een bepaalde periode is, zijn er uitzonderingen. De edelgassen (Groep 18) zijn bijvoorbeeld over het algemeen niet reactief vanwege hun volledige buitenste elektronenschillen.
 Uitputting van de ozonlaag leidt tot klimaatverandering op het zuidelijk halfrond
Uitputting van de ozonlaag leidt tot klimaatverandering op het zuidelijk halfrond Grote aardbevingen vormen landschap op grote hoogte
Grote aardbevingen vormen landschap op grote hoogte Hoe beïnvloedt water landvormen en klimaten?
Hoe beïnvloedt water landvormen en klimaten?  Echt uitgestorven of gewoon niet de moeite waard om te zoeken? Wetenschappers wilden ontdekken hoe bedreigd bepaalde soorten zijn
Echt uitgestorven of gewoon niet de moeite waard om te zoeken? Wetenschappers wilden ontdekken hoe bedreigd bepaalde soorten zijn  Bosbranden Australië laaien op terwijl hittegolf nieuwe ellende brengt
Bosbranden Australië laaien op terwijl hittegolf nieuwe ellende brengt
Hoofdlijnen
- Wat is een analogie voor cilia en flagella?
- Wat zijn variaties in specifieke nucleotiden die gekoppeld zijn aan menselijke ziekten?
- Hoeveel botten zijn er in het menselijk lichaam? Een complete gids voor het 206-botskelet
- Wat is neurobiom?
- Wat was etnische DNA -achtergrond?
- De Europese wisent kan zich goed aanpassen aan het mediterrane klimaat van Zuid-Spanje, zo blijkt uit analyse
- Wat beschrijft 2 soorten die zo nauw samenwerken dat ze aan elkaar zijn aangepast?
- Welk type wortel heeft een broodvruchten?
- Boeiende celbrochures maken:een stapsgewijze handleiding
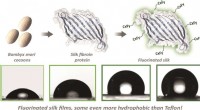
- Wetenschappers gebruiken gemodificeerde zijde-eiwitten om nieuwe anti-aanbakoppervlakken te creëren
- Kijken naar atomen die bewegen in hybride perovskietkristallen onthult aanwijzingen voor het verbeteren van zonnecellen

- Wetenschappers hebben de diversiteit van koolwaterstofmoleculen verklaard door hun magie

- Stapsgewijze handleiding voor het berekenen van moleculaire polariteit
- Onderzoekers gebruiken kunstmatige neurale netwerken om het testen van materialen te stroomlijnen

 Winst Boeing stijgt na belastingafrekening verhoogt schatting van inkomsten
Winst Boeing stijgt na belastingafrekening verhoogt schatting van inkomsten Waarom Catalyst vereist wanneer waterstof reageert met jodium?
Waarom Catalyst vereist wanneer waterstof reageert met jodium?  Eilandbewoners in de Stille Oceaan halen al lang wijsheid uit de aarde, de lucht en de golven – de wetenschap ondersteunt ze
Eilandbewoners in de Stille Oceaan halen al lang wijsheid uit de aarde, de lucht en de golven – de wetenschap ondersteunt ze  Het belang van dieren in mensenlevens
Het belang van dieren in mensenlevens Wanneer een wetenschapper zijn of haar bevindingen deelt met andere wetenschappers?
Wanneer een wetenschapper zijn of haar bevindingen deelt met andere wetenschappers?  Verband tussen het atoomnummer en de chemische reactiviteit van alkalimetalen
Verband tussen het atoomnummer en de chemische reactiviteit van alkalimetalen Wat beïnvloedt de opkomst van influencers?
Wat beïnvloedt de opkomst van influencers?  Hoe beïnvloedt zonlicht het Rainforest Biome?
Hoe beïnvloedt zonlicht het Rainforest Biome?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

