
Wetenschap
Tribromide (Br₃⁻) Moleculaire geometrie:bindingshoeken en -vorm begrijpen
* Boron's hybridisatie: Borium in tribromide heeft sp²-hybridisatie. Dit betekent dat het drie sigma-bindingen vormt, waarbij gebruik wordt gemaakt van één 2s- en twee 2p-orbitalen.
* Eenzame paren: Het centrale booratoom heeft geen alleenstaande elektronenparen.
* VSEPR-theorie: Volgens de Valence Shell Electron Pair Repulsion (VSEPR)-theorie zullen de elektronenparen rond het centrale atoom zichzelf rangschikken om afstoting te minimaliseren. In dit geval zullen de drie bindingsparen (van de broomatomen) zich zo ver mogelijk uit elkaar schikken, wat resulteert in een lineaire geometrie.
Daarom is de moleculaire geometrie van tribromide (Br₃⁻) lineair.
 Hoe biologische en chemische oorlogsvoering werkt
Hoe biologische en chemische oorlogsvoering werkt  Welke vier soorten organische moleculen worden in levende wezens aangetroffen?
Welke vier soorten organische moleculen worden in levende wezens aangetroffen?  Een groener proces voor het extraheren van verbindingen uit landbouw- en voedselafval
Een groener proces voor het extraheren van verbindingen uit landbouw- en voedselafval Geef redenen dat zuurstof een gas wordt genoemd?
Geef redenen dat zuurstof een gas wordt genoemd?  Wat is de term voor een reactie in welke substraat elektronen wint?
Wat is de term voor een reactie in welke substraat elektronen wint?
 Waarom eten herbivoren alleen planten?
Waarom eten herbivoren alleen planten?  Een nachtelijk zicht op de tropische storm Hernan vanaf een NASA-NOAA-satelliet
Een nachtelijk zicht op de tropische storm Hernan vanaf een NASA-NOAA-satelliet Paden om de geest van klimaatontkenners te veranderen
Paden om de geest van klimaatontkenners te veranderen Algenplaag roept twijfels op over vrijwillige preventie van afspoeling
Algenplaag roept twijfels op over vrijwillige preventie van afspoeling Droogte trof in 2018 ongeveer 90% van het Duitse grondgebied
Droogte trof in 2018 ongeveer 90% van het Duitse grondgebied
Hoofdlijnen
- Kan een sleutel worden gebruikt om organismen te identificeren?
- Darwins vier kernprincipes van evolutie uitgelegd
- Wat was de bruine klodder die zich vormde in het Stanley-laboratoriumexperiment?
- Wat is Gene Linkage?
- Wat is het proces waarmee grote deeltjes in cel kunnen worden genomen voor voedselbescherming van het lichaam of het weggooien van oude dode cellen die worden genoemd?
- Wat is een structuur in de cel die bepaalde functioneert?
- Wat zijn bèta -deeltjes?
- Het aantal chromosomen in een octopus eiercel zal wat zijn?
- Methoden voor het ontwikkelen van organismen met gewenste eigenschappen?
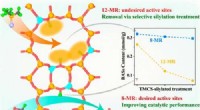
- Nieuwe strategie om de verspreiding van zuurplaatsen in zeolieten te beheersen
- Waarom bepaalde ijsjes bestand zijn tegen smelten:een wetenschappelijke verklaring

- Oxidatie in nieuw coatingmateriaal voor gasturbinemotoren van vliegtuigen
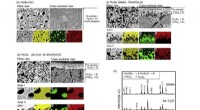
- Database voor stegananalyse van forensisch bewijs

- Vorming van celmembraancomponentdomeinen in kunstmatige lipidedubbellaag

 Als de zon boven het hoofd staat bij Tropic of Steenbok Places op Arctic Circle heeft?
Als de zon boven het hoofd staat bij Tropic of Steenbok Places op Arctic Circle heeft?  Hypersonische materiegolven voor ultrasnelle atomtronica
Hypersonische materiegolven voor ultrasnelle atomtronica Hoe verandert metamorfe rots naar sediment?
Hoe verandert metamorfe rots naar sediment?  De leiding nemen, wijnliefhebbers, en vertrouw op je smaakpapillen
De leiding nemen, wijnliefhebbers, en vertrouw op je smaakpapillen Waarom is gevleugelde boon dicot?
Waarom is gevleugelde boon dicot?  Welke twee eigenschappen hebben alle krachten?
Welke twee eigenschappen hebben alle krachten?  Hoe heeft de wetenschap zijn naam gekregen?
Hoe heeft de wetenschap zijn naam gekregen?  Welk gen wordt gemaskeerd als het gepaard gaat met een dominant gen?
Welk gen wordt gemaskeerd als het gepaard gaat met een dominant gen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

