
Wetenschap
Stapsgewijze handleiding voor het berekenen van moleculaire polariteit
Door David Ward Bijgewerkt op 24 maart 2022
Een scheikundige kan vaak voorspellen of een molecuul polair is door rekening te houden met de elektronegativiteit van de atomen waaruit het bestaat. Een nauwkeurige bepaling van het dipoolmoment van een molecuul vereist echter een nauwkeurige beschrijving van de geometrie ervan en de toepassing van vectoroptelling. Bij deze methode wordt elke binding weergegeven door een vector waarvan de grootte het verschil in elektronegativiteit weerspiegelt en waarvan de richting de oriëntatie van de binding binnen de driedimensionale vorm volgt.
Stap 1
Teken het molecuul in een standaard Lewis-structuur, inclusief alle atomen en alleenstaande paren. Deze visuele weergave vormt de basis voor daaropvolgende analyse.
Stap 2
Bepaal de moleculaire geometrie. Veel voorkomende vormen zijn:
- Lineair – één of twee gebonden atomen.
- Hoekig – twee gebonden atomen met losse paren.
- Trigonaal vlak – drie gebonden atomen zonder alleenstaande paren.
- Trigonaal piramidaal – drie gebonden atomen met een eenzaam paar.
- Tetraëdrisch – vier gebonden atomen.
Stap 3
Wijs elektronegativiteitswaarden (Pauling-schaal) toe aan elk atoom. De grootte van elke vector zal evenredig zijn met het elektronegativiteitsverschil tussen de gebonden atomen. Een C–O-binding (2,5Pauling-eenheden) zou bijvoorbeeld een langere vector genereren dan een C–H-binding (1,0Pauling-eenheden).
Stap 4
Teken een vector voor elke binding, waarbij de lengte wordt bepaald door het elektronegativiteitsverschil en de richting wordt bepaald door de oriëntatie van de binding in de moleculaire vorm. Zorg ervoor dat de vectoren zo zijn gepositioneerd dat hun staart naar het gedeelde elektronenpaar wijst.
Stap 5
Voer vectoroptelling uit door de vectoren van begin tot eind uit te lijnen. De resulterende vector, gemeten vanaf de oorsprong tot het vrije uiteinde, vertegenwoordigt het dipoolmoment van het molecuul. Een niet-nul resultante geeft polariteit aan; de grootte ervan komt overeen met de dipoolsterkte, en de richting wijst naar de meer elektronegatieve kant.
TL;DR (te lang; niet gelezen)
Gemeenschappelijke moleculen hebben vaak dipoolmomenten gepubliceerd. Let bij het schatten van de polariteit op zeer elektronegatieve atomen zoals zuurstof of fluor aan één kant van de structuur. Hun aanwezigheid aan één kant creëert doorgaans een netto dipool in die richting.
Waarschuwing
Het berekenen van dipoolmomenten wordt steeds complexer voor grotere moleculen en wordt meestal uitgevoerd met computationele chemiesoftware. De hier geschetste vectormethode is het meest geschikt voor kleine, eenvoudige moleculen.
 N-gedoteerde koolstof-ingekapselde overgangsmetaalkatalysatoren om de prestaties van zink-luchtbatterijen te optimaliseren
N-gedoteerde koolstof-ingekapselde overgangsmetaalkatalysatoren om de prestaties van zink-luchtbatterijen te optimaliseren Een blauw pigment dat een hoogwaardig ammoniakadsorbens blijkt te zijn
Een blauw pigment dat een hoogwaardig ammoniakadsorbens blijkt te zijn Wat is de naam van CaO3 van het samengestelde?
Wat is de naam van CaO3 van het samengestelde?  Hoeveel zuurstofatomen zijn er in 1 molecuul van CA OH 2?
Hoeveel zuurstofatomen zijn er in 1 molecuul van CA OH 2?  Wat is de meest zure pH 2 5 7 of 11?
Wat is de meest zure pH 2 5 7 of 11?
 Groot-Brittannië publiceert langverwacht luchtvervuilingsplan
Groot-Brittannië publiceert langverwacht luchtvervuilingsplan De voordelen en nadelen van niet-hernieuwbare energiebronnen
De voordelen en nadelen van niet-hernieuwbare energiebronnen De VS zegt dat twee forever-chemicaliën gevaarlijk zijn en zegt tegen de vervuilers dat ze moeten betalen
De VS zegt dat twee forever-chemicaliën gevaarlijk zijn en zegt tegen de vervuilers dat ze moeten betalen  Nieuwe app om landbouwgrond te beoordelen en de kwaliteit ervan te verbeteren
Nieuwe app om landbouwgrond te beoordelen en de kwaliteit ervan te verbeteren orkanen, overstromingsverzekering en de gevaren van business as usual
orkanen, overstromingsverzekering en de gevaren van business as usual
Hoofdlijnen
- Is het mogelijk om een knock -out mutantplant te hebben die geen zichtbaar fenotype vertoont, verschilt van de wildtype plant?
- Wat is ATP7B -gen?
- Nucleotiden zijn gemaakt van een suiker genaamd wat?
- Welke orgaansystemen worden gebruikt als we eten?
- Wat doet een kern in plantencel?
- Welke term wordt gebruikt om organismen te beschrijven die over vele generaties dezelfde vorm van een eigenschap hebben doorgegeven?
- Wat zijn de huidige doelen van Human Genome Project?
- Welk element wordt als het meest veelzijdig beschouwd in levende organismen en waarom?
- Wat is de naam van cel -eiwitten en een lipide dubbellaagse barrière?
- Veilige minerale olierook creëren voor film- en veiligheidstoepassingen

- Waterontharder:voordelen, nadelen en wanneer u deze moet kiezen

- Nieuwe studie stelt lage kosten voor, maskerontwerp met hoog rendement

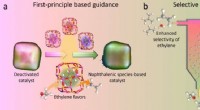
- Onderzoekers regenereren gedeactiveerde katalysator in het proces van methanol tot olefinen
- Synthetische moleculaire codes programmeren om genen aan te zetten
 Wat is de formule voor sulfaat?
Wat is de formule voor sulfaat?  Welke gebeurtenissen bij een transformatiegrens helpen metamorfe rotsen te vormen?
Welke gebeurtenissen bij een transformatiegrens helpen metamorfe rotsen te vormen?  Siliciumdioxide reageert met natriumhydroxide om wat te produceren?
Siliciumdioxide reageert met natriumhydroxide om wat te produceren?  Waar is het vouwen van Galtee Mountains ontstaan?
Waar is het vouwen van Galtee Mountains ontstaan?  Wat is deze witte blanco de blauwe witte hete kern van een ster die achterliet nadat de buitenste lagen zijn uitgebreid en in de ruimte zijn uitgegrepen?
Wat is deze witte blanco de blauwe witte hete kern van een ster die achterliet nadat de buitenste lagen zijn uitgebreid en in de ruimte zijn uitgegrepen?  Mini-elektriciteitsgenerator gemaakt van kwantumstippen
Mini-elektriciteitsgenerator gemaakt van kwantumstippen Wereldprimeur die bouwstenen levert voor nieuwe nano-apparaten
Wereldprimeur die bouwstenen levert voor nieuwe nano-apparaten Wat is de vorm van verre?
Wat is de vorm van verre?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

