
Wetenschap
Ionische bindingen begrijpen:de rol van elektronegativiteit
Elektronegativiteit:de aantrekkingskracht op elektronen
* Definitie: Elektronegativiteit is een maatstaf voor het vermogen van een atoom om elektronen binnen een chemische binding aan te trekken.
* Trends: Elektronegativiteit neemt over het algemeen toe over een periode (van links naar rechts) en neemt af in een groep op het periodiek systeem.
Wat er gebeurt als er een groot verschil is
* Sterkere aantrekkingskracht: Wanneer twee atomen met een groot verschil in elektronegativiteit een binding aangaan, oefent het atoom met de hogere elektronegativiteit een veel sterkere aantrekkingskracht uit op de gedeelde elektronen.
* Elektronenoverdracht: Deze sterke aantrekkingskracht is zo groot dat het meer elektronegatieve atoom in wezen het elektron (de elektronen) van het minder elektronegatieve atoom "steelt".
* Ionen: Deze elektronenoverdracht creëert ionen:
* Het atoom dat elektronen opneemt, wordt negatief geladen (anion).
*Het atoom dat elektronen verliest, wordt positief geladen (kation).
Het resultaat:ionenbindingen
* Elektrostatische aantrekkingskracht: Tegengestelde ladingen trekken elkaar aan! De sterke elektrostatische aantrekkingskracht tussen het positief geladen kation en het negatief geladen anion creëert een ionische binding.
* Vorming van kristallen: Ionische verbindingen vormen doorgaans kristallijne structuren waarin ionen in een regelmatig, herhalend patroon zijn gerangschikt om de elektrostatische aantrekkingskracht te maximaliseren.
Voorbeeld:
Natrium (Na) heeft een lage elektronegativiteit, terwijl chloor (Cl) een hoge elektronegativiteit heeft. Wanneer ze binden, trekt chloor het elektron uit natrium, waardoor een Na⁺-ion en een Cl⁻-ion ontstaan. De sterke aantrekkingskracht tussen deze ionen vormt de ionische verbinding natriumchloride (NaCl), algemeen bekend als keukenzout.
Belangrijkste afhaalmaaltijden: Grote verschillen in elektronegativiteit leiden tot een volledige overdracht van elektronen, resulterend in de vorming van ionen en de sterke elektrostatische aantrekkingskracht die ionische binding definieert.
 Onderzoek laat zien hoe C:N:P-stoichiometrie reageert op landbouwgrondgebruik en klimaat
Onderzoek laat zien hoe C:N:P-stoichiometrie reageert op landbouwgrondgebruik en klimaat  Wat is uniek aan sfeer?
Wat is uniek aan sfeer?  Feds kondigen historische waterbezuinigingen aan:wat betekent dit?
Feds kondigen historische waterbezuinigingen aan:wat betekent dit? Op zoek naar vingerafdrukken op het snijvlak van weer en klimaat
Op zoek naar vingerafdrukken op het snijvlak van weer en klimaat Onderzoek toont aan hoe espenbossen de diversiteit behouden die nodig is om zich aan te passen aan veranderende omgevingen
Onderzoek toont aan hoe espenbossen de diversiteit behouden die nodig is om zich aan te passen aan veranderende omgevingen
Hoofdlijnen
- Hoe de bescherming van de gezondheid van planten essentieel is voor toekomstige welvaart en duurzaamheid
- Hoe zou u de kenmerken van discicristaten beschrijven?
- Wat is hetzelfde van DNA en RNA?
- Wat is de Western Blot-test?
- Overeenkomsten van mitose en meiose
- Worden de sporen geproduceerd door mos sporophyt gevormd meiose of mitose?
- Hoe verschilt RNA van DNA -lijst 3 dingen?
- Hoe veranderde de evolutietheorie de manier waarop biologen over classificatie dachten?
- Hoe zijn meercellige organismen efficiënter dan eencellige organismen?
- Plantaardige verbinding zou een sleutelrol kunnen spelen bij het bestrijden van de ziekte van Alzheimer

- Belangrijke rol van singletzuurstof in synergetisch antimicrobieel mechanisme

- Nieuwe moleculen afgeleid van cannabidiol zijn ontworpen met krachtigere antioxidanten

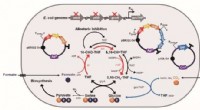
- Gemanipuleerde E. coli met mierenzuur en CO2 als een C1-raffinaderijplatformstam
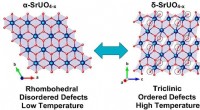
- Uranium gebruiken om orde te scheppen in wanorde
 Draaiende beweging creëert een lichtschakeleffect bij Uranus
Draaiende beweging creëert een lichtschakeleffect bij Uranus Hoe kun je sterren zien als ze miljoenen lichtjaren weg zijn?
Hoe kun je sterren zien als ze miljoenen lichtjaren weg zijn?  Wat doen evenwichtige krachten naar een object?
Wat doen evenwichtige krachten naar een object?  Slechts 1 op de 5 hoofdredacteuren van toonaangevende medische tijdschriften is vrouw, studie vondsten
Slechts 1 op de 5 hoofdredacteuren van toonaangevende medische tijdschriften is vrouw, studie vondsten Wat is autobiologie?
Wat is autobiologie?  Ideologie is niet de belangrijkste factor die kinderen ertoe aanzet zich bij terroristische groeperingen aan te sluiten
Ideologie is niet de belangrijkste factor die kinderen ertoe aanzet zich bij terroristische groeperingen aan te sluiten Wat is het meest voorkomende metalen element in de lithosfeer?
Wat is het meest voorkomende metalen element in de lithosfeer?  Welke vormreceptorsites op het post -synaptische celmembraan?
Welke vormreceptorsites op het post -synaptische celmembraan?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

