
Wetenschap
Zwavelzuur:zuur of base? De eigenschappen ervan begrijpen
Zwavelzuur (H₂SO₄) is niet een Brønsted-basis. Het is een Brønsted-zuur .
Dit is waarom:
* Brønsted-Lowry zuur: Een Brønsted-Lowry-zuur is een stof die een proton (H⁺) doneert. Zwavelzuur doneert gemakkelijk twee protonen, waardoor het een sterk diprotisch zuur wordt.
* Brønsted-Lowry-basis: Een Brønsted-Lowry-base is een stof die een proton accepteert. Zwavelzuur accepteert geen protonen, maar doneert ze.
Voorbeeld:
Wanneer zwavelzuur reageert met water, doneert het een proton aan water en vormt het hydroniumion (H₃O⁺) en het bisulfaation (HSO₄⁻):
H₂SO₄ + H₂O → H₃O⁺ + HSO₄⁻
Deze reactie toont aan dat zwavelzuur werkt als een Brønsted-zuur door een proton te doneren.
 Onderzoekers laten zien hoe calciumionen natriumionenkanalen in celmembranen kunnen blokkeren
Onderzoekers laten zien hoe calciumionen natriumionenkanalen in celmembranen kunnen blokkeren  Wat is een aluminium auto -body samengesteld element of mengsel?
Wat is een aluminium auto -body samengesteld element of mengsel?  Hoe verschillen synthese enkele vervanging en dubbele reacties?
Hoe verschillen synthese enkele vervanging en dubbele reacties?  Wat is de dichtheid van Vigigar?
Wat is de dichtheid van Vigigar?  Welke chemicaliën worden geproduceerd wanneer een zuur reageert met een metaalcarbonaat of hydroxide?
Welke chemicaliën worden geproduceerd wanneer een zuur reageert met een metaalcarbonaat of hydroxide?
 Overstappen naar een schone economie kan Australië honderden miljarden besparen, vondsten melden
Overstappen naar een schone economie kan Australië honderden miljarden besparen, vondsten melden Wat leren leerlingen van klasse 7 in de wetenschap?
Wat leren leerlingen van klasse 7 in de wetenschap?  Klimaatbeloften van grote bedrijven zijn kritisch onvoldoende:rapport
Klimaatbeloften van grote bedrijven zijn kritisch onvoldoende:rapport  De ontziltingslozing van Sydney verhoogt het leven van vissen in tijden van klimaatonzekerheid
De ontziltingslozing van Sydney verhoogt het leven van vissen in tijden van klimaatonzekerheid Studie bevestigt bliksem krachtiger over oceaan dan over land
Studie bevestigt bliksem krachtiger over oceaan dan over land
Hoofdlijnen
- Waar wordt het DNA geplaatst in gelelektrofoesis -apparaat?
- Hoe zou u een microscoop kunnen gebruiken om te bepalen of het monster leven of niet-levend is?
- De nieuwsgierigheid van cichliden bevordert de biodiversiteit:hoe verkennend gedrag helpt bij ecologische aanpassing
- Dit is de reden waarom walvissen niet verdrinken als ze voedsel onder water opslokken
- Meer dan 1,1 miljoen zeeschildpadden gestroopt in de afgelopen drie decennia:studie
- Genomics onthult hoe concurrentie tussen bacteriën de impact van vaccinatie beïnvloedt
- Welk proces stopt wanneer een ribosoom het stopcodon bereikt?
- Welk deel van een celmembraan is hydrofoob?
- Wat zijn de basisstoffen waaruit een cel bestaat?
- Wetenschappers verbeteren de analyse van röntgengegevens met kunstmatige intelligentie

- Elektrisch geleidende verven en andere polymeerlegeringen nu gemakkelijk te produceren

- Nieuwe methode om composieten te maken met vormgeheugen

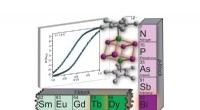
- Onderzoekers maken een magneet gemaakt van één molecuul
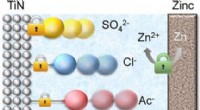
- Zink-ion hybride condensatoren met ideale anionen in de elektrolyt vertonen extra lange prestaties
 Waarom zijn ringen zo merkbaar in vergelijking met andere planeten ons zonnestelsel?
Waarom zijn ringen zo merkbaar in vergelijking met andere planeten ons zonnestelsel?  Wat voor soort energie breidt een ballon uit?
Wat voor soort energie breidt een ballon uit?  De bosbranden in de zomer waar je niets over hoorde, en de invasieve soorten die hen van brandstof voorzien
De bosbranden in de zomer waar je niets over hoorde, en de invasieve soorten die hen van brandstof voorzien Wat wordt er in rotsformaties gevonden die miljoenen jaren oud zijn?
Wat wordt er in rotsformaties gevonden die miljoenen jaren oud zijn?  Welke verbindingen zijn de meest stabiele AGCI CUCI2 AICI3 of LICI?
Welke verbindingen zijn de meest stabiele AGCI CUCI2 AICI3 of LICI?  Hoeveel mol ionen worden er geproduceerd als 2 mol Na2CO3 dissocieert?
Hoeveel mol ionen worden er geproduceerd als 2 mol Na2CO3 dissocieert?  De kloof dichten:burgerwetenschap voor het monitoren van duurzame ontwikkeling
De kloof dichten:burgerwetenschap voor het monitoren van duurzame ontwikkeling Onderzoekers ontdekken heetste lava die in de afgelopen 2,5 miljard jaar is uitgebarsten
Onderzoekers ontdekken heetste lava die in de afgelopen 2,5 miljard jaar is uitgebarsten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

