
Wetenschap
Covalente obligaties begrijpen:vorming, structuur en delen
1. Atoomstructuur:
* Elektronen: Atomen hebben negatief geladen elektronen die rond hun kern cirkelen. Elektronen bevinden zich in energieniveaus die schillen worden genoemd. De buitenste schil, de valentieschil genoemd, is cruciaal voor de binding.
* Stabiliteit: Atomen streven naar een stabiele configuratie, meestal met een volledige buitenschil (meestal 8 elektronen, ook wel de octetregel genoemd).
2. Elektronen delen:
* Wanneer atomen met onvolledige valentieschillen elkaar ontmoeten, kunnen ze elektronen delen om een stabiele configuratie te bereiken.
* Dit delen resulteert in een covalente band , waar de gedeelde elektronen worden aangetrokken door de kernen van beide atomen, waardoor ze bij elkaar worden gehouden.
3. Soorten covalente obligaties:
* Enkele obligatie: Eén paar elektronen wordt gedeeld tussen twee atomen.
* Dubbele obligatie: Twee elektronenparen worden gedeeld tussen twee atomen.
* Triple Bond: Drie elektronenparen worden gedeeld tussen twee atomen.
Voorbeeld:water (H₂O)
* Zuurstof heeft 6 elektronen in de buitenste schil en heeft er nog 2 nodig om stabiliteit te bereiken.
*Elk waterstofatoom heeft 1 elektron in zijn buitenste schil en heeft er nog 1 nodig.
* Zuurstof deelt één elektron met elk waterstofatoom en vormt twee enkele covalente bindingen. Hierdoor zijn de buitenste schillen van alle betrokken atomen compleet, waardoor het molecuul stabiel wordt.
Belangrijkste eigenschappen van covalente obligaties:
* Sterk: Covalente bindingen zijn sterk en vereisen aanzienlijke energie om te breken.
* Richting: De gedeelde elektronen zijn gelokaliseerd tussen de gebonden atomen, waardoor een specifieke directionaliteit ontstaat.
* Niet-polair versus polair:
* Niet-polair: Elektronen worden gelijkelijk verdeeld tussen atomen met vergelijkbare elektronegativiteit.
* Polair: Elektronen worden ongelijk verdeeld tussen atomen met verschillende elektronegativiteit, waardoor gedeeltelijke ladingen ontstaan.
Samenvattend worden covalente bindingen gevormd door het delen van elektronen tussen atomen om een stabiele configuratie te bereiken. Door dit delen ontstaat een sterke en doelgerichte band die een cruciale rol speelt bij de vorming van moleculen.
 Hoe de atoomstructuur van atomen
Hoe de atoomstructuur van atomen Hoe het dodelijke gif van de kegelslak ons kan helpen betere medicijnen te maken
Hoe het dodelijke gif van de kegelslak ons kan helpen betere medicijnen te maken  Wat zijn de chemische eigenschappen van cement?
Wat zijn de chemische eigenschappen van cement?  Wat zijn overeenkomsten en verschillen tussen fysische chemische verwering?
Wat zijn overeenkomsten en verschillen tussen fysische chemische verwering?  Chemische verandering:definitie, voorbeelden en toepassingen in de echte wereld
Chemische verandering:definitie, voorbeelden en toepassingen in de echte wereld
 Ontbossing kan de bosbranden in het Amazonewoud elk jaar verergeren
Ontbossing kan de bosbranden in het Amazonewoud elk jaar verergeren Hoe ver reizen invasieve soorten?
Hoe ver reizen invasieve soorten?  De hoofdstad van Zimbabwe droogt op door het afsluiten van de kraan voor 2 miljoen mensen
De hoofdstad van Zimbabwe droogt op door het afsluiten van de kraan voor 2 miljoen mensen Toen dinosaurussen verdwenen, bossen bloeiden
Toen dinosaurussen verdwenen, bossen bloeiden Onderzoekers analyseren 125 verbindingen van olie die in de Golf van Mexico is gemorst om hun levensduur te bepalen
Onderzoekers analyseren 125 verbindingen van olie die in de Golf van Mexico is gemorst om hun levensduur te bepalen
Hoofdlijnen
- Wat zijn de vier belangrijkste functies van het menselijk lichaam?
- Chimpansees in het wild passen waarschuwingen aan op basis van wat anderen in hun groep al weten, zo blijkt uit onderzoek
- Wanneer de vulgreep wordt gebruikt om een cel aangrenzende cellen te kopiëren die wordt genoemd?
- Waarom is ATP belangrijk voor cellulaire ademhaling?
- Welke structuur in de cel is chemische messenger voor DNA?
- Wat zijn de namen van twee soorten autotrofen?
- Twee muziekbloemlezingen nu voor eeuwig opgeslagen in DNA
- Wat voor soort banen kun je krijgen met een graad in fysiologie?
- Wat wordt er in de zijkanten van DNA -moleculen gevonden, maar niet op sporten?
- Nieuwe supramoleculaire copolymeren aangedreven door zelfsortering van moleculen

- Waarom warm water minder dicht is dan koud water:de wetenschap erachter

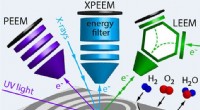
- Drie microscopen zien meer dan twee
- Onderzoekers vinden nieuwe suikervervangers in citrus die de voedings- en drankenindustrie kunnen veranderen

- Samenwerking vormt de strategie voor het vasthouden van extracellulaire blaasjes
 Wat is de metrische schaal?
Wat is de metrische schaal?  Hoe verkrijgt het organisme energie?
Hoe verkrijgt het organisme energie?  Groenten irrigeren met afvalwater in Afrikaanse steden kan ziektes verspreiden
Groenten irrigeren met afvalwater in Afrikaanse steden kan ziektes verspreiden Herinnering aan dingen uit het verleden beïnvloedt hoe vrouwelijke veldkrekels partners selecteren
Herinnering aan dingen uit het verleden beïnvloedt hoe vrouwelijke veldkrekels partners selecteren  Wat geldt voor verplaatsing 1. Het kan niet nul zijn 2. De grootte ervan groter dan de afstand die door object wordt afgelegd?
Wat geldt voor verplaatsing 1. Het kan niet nul zijn 2. De grootte ervan groter dan de afstand die door object wordt afgelegd?  Laat CEO's deelnemen aan dezelfde pensioenregeling als het personeel om het te helpen beschermen, zeggen experts
Laat CEO's deelnemen aan dezelfde pensioenregeling als het personeel om het te helpen beschermen, zeggen experts Hoe wordt voedsel omgezet in het lichaam?
Hoe wordt voedsel omgezet in het lichaam?  Samengesteld uit aminozuren met lange ketens?
Samengesteld uit aminozuren met lange ketens?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

