
Wetenschap
Chemische binding begrijpen:waarom atomen bindingen vormen
* Octetregel: De meeste atomen zijn het meest stabiel als ze acht elektronen in hun buitenste schil (valentieschil) hebben. Dit staat bekend als de octetregel. Er bestaan uitzonderingen, vooral voor kleinere atomen zoals waterstof en helium die streven naar een duet (2 elektronen).
* Elektronegativiteit: Atomen met een hogere elektronegativiteit hebben een sterkere aantrekkingskracht op elektronen. Dit verschil in elektronegativiteit stimuleert de vorming van bindingen.
* Stabiliteit: Door elektronen te delen of over te dragen, kunnen atomen een volledige buitenste schil bereiken, wat resulteert in een stabielere configuratie met lagere energie. Deze stabiliteit is de drijvende kracht achter chemische binding.
Soorten chemische bindingen
* Ionische bindingen: Gevormd wanneer een atoom een elektron overdraagt aan een ander atoom. Dit resulteert in de vorming van tegengesteld geladen ionen die elkaar aantrekken.
* Covalente obligaties: Gevormd wanneer twee atomen elektronen delen. Door dit delen kunnen beide atomen een stabiele elektronenconfiguratie bereiken.
* Metaalverbindingen: Gevonden in metalen. Elektronen zijn gedelokaliseerd en kunnen vrij door de metalen structuur bewegen.
Waarom edelgassen stabiel zijn
Edelgassen, zoals helium, neon en argon, zijn al stabiel. Ze hebben een volledige buitenste schil van elektronen, waardoor ze niet-reactief en chemisch inert zijn.
Samenvattend binden atomen zich met elkaar om een stabielere elektronenconfiguratie te bereiken, zoals die van de edelgassen. Deze stabiliteit wordt bereikt door het delen of overbrengen van elektronen, wat resulteert in de vorming van verschillende soorten chemische bindingen.
 Wat zijn de goede dingen en slecht aan de bodem?
Wat zijn de goede dingen en slecht aan de bodem?  Waarom koala's nog leven:een diepe duik in hun overleving tijdens de klimaatcrisis
Waarom koala's nog leven:een diepe duik in hun overleving tijdens de klimaatcrisis  Afbrekers in de Noordpool
Afbrekers in de Noordpool GRACE-missiegegevens dragen bij aan ons begrip van klimaatverandering
GRACE-missiegegevens dragen bij aan ons begrip van klimaatverandering Wat is de rol van een cactus terwijl deze energie en materie door zijn ecosysteem verplaatst?
Wat is de rol van een cactus terwijl deze energie en materie door zijn ecosysteem verplaatst?
Hoofdlijnen
- Wat betekent het om een enzym te denatureren?
- Hoe ziet een menselijke cel eruit?
- Wat is het verschil tussen biotische en abiotische factoren geven een voorbeeld van elk?
- Welke hormoonachtige moleculen worden NIET uit arachidonzuur geproduceerd?
- Welk deel van de bloem waar eten wordt opgeslagen als zetmeel?
- Wat is het ding dat mannelijk deel van de plant bevat?
- Waarom leven sommige microben in je darmen en andere niet?
- Wat is bio-activiteit?
- Wat produceert eiwitten in een cel?
- Het verhaal achter oneindig recyclebaar plastic

- Lichtgestuurde nanomachine regelt katalyse
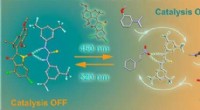
- Kun je een malt whisky van 10 jaar maken in weken? De chemie zegt ja

- Molecular activity painting om schakelaarachtige, lichtgestuurde verstoringen in cellen
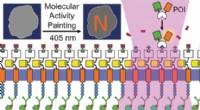
- Onderzoekers krijgen inzicht in hoe enzymen specifieke reacties bereiken
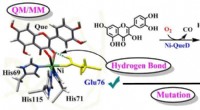
 Polikarpov I-16
Polikarpov I-16  Hoe meet je de dichtheid van een onregelmatig object dat niet drijft?
Hoe meet je de dichtheid van een onregelmatig object dat niet drijft?  Hoe wordt Apollo normaal afgebeeld?
Hoe wordt Apollo normaal afgebeeld?  Wat maken wetenschappers op basis van hun observaties?
Wat maken wetenschappers op basis van hun observaties?  Een kracht van 30 N wordt toegepast op een object dat vervolgens versnelt op 3 m S2 Wat de massa object?
Een kracht van 30 N wordt toegepast op een object dat vervolgens versnelt op 3 m S2 Wat de massa object?  Wat zijn drie kenmerken die alle organismen hebben?
Wat zijn drie kenmerken die alle organismen hebben?  Tesla richt Shanghai-bedrijf op terwijl het de aanwezigheid in China uitbreidt
Tesla richt Shanghai-bedrijf op terwijl het de aanwezigheid in China uitbreidt Studie vindt het veranderen van opgeloste organische koolstof in de meren van Maine van cruciaal belang voor het behoud van de drinkwaterkwaliteit
Studie vindt het veranderen van opgeloste organische koolstof in de meren van Maine van cruciaal belang voor het behoud van de drinkwaterkwaliteit
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

