
Wetenschap
Chemische bindingen begrijpen:waarom atomen ze vormen
1. Octetregel:
* De meeste atomen streven naar een volledige buitenste schil van elektronen (meestal 8, vandaar de "octetregel"). Deze configuratie geeft ze een stabiele, energiezuinige toestand.
* Atomen met onvolledige buitenste schillen zijn minder stabiel en reactiever.
2. Elektrostatische interacties:
* Chemische bindingen ontstaan door elektrostatische interacties tussen atomen.
* Deze interacties kunnen zijn:
* Aantrekkelijk: tussen tegengesteld geladen deeltjes (elektronen en protonen)
* Weerzinwekkend: tussen gelijkgeladen deeltjes
3. Soorten chemische bindingen:
* Ionische bindingen: gevormd door de overdracht van elektronen tussen atomen, waardoor ionen (geladen deeltjes) ontstaan die tot elkaar worden aangetrokken.
* Covalente bindingen: gevormd door het delen van elektronen tussen atomen, waarbij beide atomen profiteren van de gedeelde elektronen en hun buitenste schillen vullen.
* Metaalverbindingen: gevormd door het delen van elektronen tussen een rooster van metaalatomen. Hierdoor ontstaat een ‘zee van elektronen’ die verantwoordelijk is voor de unieke eigenschappen van metalen, zoals geleidbaarheid.
4. Voorbeelden:
* Natrium (Na) en chloor (Cl): Natrium heeft één elektron in zijn buitenste schil, terwijl chloor er nog één nodig heeft om zijn octet te voltooien. Natrium *doneert* zijn elektron aan chloor, waardoor een positief geladen natriumion (Na+) en een negatief geladen chloride-ion (Cl-) ontstaat, die tot elkaar worden aangetrokken en een ionische binding vormen.
* Waterstof (H) en zuurstof (O): Elk waterstofatoom heeft één elektron nodig om zijn buitenste schil te voltooien, en zuurstof heeft er twee nodig. Ze delen elektronen en vormen covalente bindingen in een watermolecuul (H2O).
Samengevat:
Atomen vormen chemische bindingen om een stabielere, lagere energietoestand te bereiken. Ze doen dit door elektronen te winnen, te verliezen of te delen om hun buitenste schillen te vullen en hun totale energie te minimaliseren. Het type binding dat wordt gevormd, hangt af van de specifieke eigenschappen van de betrokken atomen.
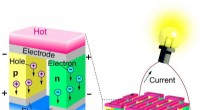
 Terahertz-golven onthullen verborgen processen in ultrasnelle kunstmatige fotosynthese
Terahertz-golven onthullen verborgen processen in ultrasnelle kunstmatige fotosynthese NIST dringt aan op voorzichtigheid bij het gebruik van bewijsmateriaal in de rechtszaal
NIST dringt aan op voorzichtigheid bij het gebruik van bewijsmateriaal in de rechtszaal Wat zijn de belangrijke vragen in het tweedejaars scheikunde?
Wat zijn de belangrijke vragen in het tweedejaars scheikunde?  Zijn natriumpolyacrylaat en percarbonaat hetzelfde?
Zijn natriumpolyacrylaat en percarbonaat hetzelfde?  Noem twee fysieke eigenschappen van niet -metalen?
Noem twee fysieke eigenschappen van niet -metalen?
 Nieuwe tool voor het beoordelen van de voordelen, risico's en duurzaamheid van de visconsumptie
Nieuwe tool voor het beoordelen van de voordelen, risico's en duurzaamheid van de visconsumptie Democraten en Republikeinen trekken verschillende conclusies wanneer de seizoenen te warm of te koud zijn
Democraten en Republikeinen trekken verschillende conclusies wanneer de seizoenen te warm of te koud zijn Grote overstromingen in Manilla terwijl tyfoon Filipijnen teistert
Grote overstromingen in Manilla terwijl tyfoon Filipijnen teistert NASA ziet tropische depressie 33W de Suluzee binnenkomen
NASA ziet tropische depressie 33W de Suluzee binnenkomen Klimaatverandering kan leiden tot grotere algenbloei
Klimaatverandering kan leiden tot grotere algenbloei
Hoofdlijnen
- Wat zijn de rudimentaire vormen van bacteriën?
- Wat is de term die het tegenovergestelde van dorsaal betekent?
- Wat is het doel van eiwitkatabolisme?
- Wat is een andere naam voor een specifiek verdedigingssysteem?
- Voedselketens:hoe energie door ecosystemen stroomt en waarom ze ertoe doen
- Hoe heet een paar overeenkomstige chromosomen?
- Wat doodt de Minnesota-eland? Onderzoekers lanceren nieuwe inspanningen om erachter te komen
- AI ontcijfert nieuwe genregulerende code in planten en maakt nauwkeurige voorspellingen voor nieuw gesequenced genomen
- Waarom hebben enzymen water nodig?
- Schakelen van meerdere halfgeleiders om de thermo-elektrische omzetting van afvalwarmte te stimuleren
- Binnen een atoom:de locaties van protonen, neutronen en elektronen

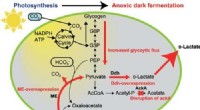
- Methode levert een hoog percentage D-lactaat op met behulp van cyanobacteriën, kan een revolutie teweegbrengen in de productie van bioplastic
- Moleculaire motor:vier rotatietoestanden
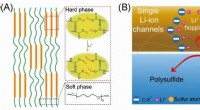
- Stabiliserende zwavelkathode door enkelvoudig Li-ionkanaalpolymeerbindmiddel
 Stazakken van hernieuwbare grondstoffen en nanocellulose
Stazakken van hernieuwbare grondstoffen en nanocellulose Wat betekenen subvorticies als kenmerken van een tornado?
Wat betekenen subvorticies als kenmerken van een tornado?  Ongrijpbare HIV-vormverandering onthuld; Belangrijke aanwijzing voor hoe virussen cellen infecteren
Ongrijpbare HIV-vormverandering onthuld; Belangrijke aanwijzing voor hoe virussen cellen infecteren  Hoeveel DNA kan bij een mens worden gevonden?
Hoeveel DNA kan bij een mens worden gevonden?  De voor- en nadelen van het gebruik van een telescoop op de grond
De voor- en nadelen van het gebruik van een telescoop op de grond  Planten en dieren van het Quartair tijdperk
Planten en dieren van het Quartair tijdperk  Geavanceerde microscopie gebruiken om nieuwe materialen voor computers en elektronica te nano-engineeren
Geavanceerde microscopie gebruiken om nieuwe materialen voor computers en elektronica te nano-engineeren Het risico op depressie en zelfmoord verdubbelt bij middelbare scholieren die te maken hebben met woningnood
Het risico op depressie en zelfmoord verdubbelt bij middelbare scholieren die te maken hebben met woningnood
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

