
Wetenschap
De broosheid van ionische verbindingen begrijpen:krachten en structuur
* Sterke elektrostatische krachten: Ionische verbindingen worden bij elkaar gehouden door sterke elektrostatische aantrekkingen tussen positief geladen kationen en negatief geladen anionen. Deze krachten zijn sterk en werken in alle richtingen, waardoor een stijve roosterstructuur ontstaat.
* Vaste posities: De ionen worden op vaste posities binnen het rooster vastgehouden en missen het vermogen om langs elkaar heen te glijden.
* Stress en roosterverstoring: Wanneer een externe kracht op een ionisch kristal wordt uitgeoefend, worden de ionen uit hun positie geduwd. Dit verstoort het evenwicht tussen aantrekkende en afstotende krachten, waardoor het rooster gemakkelijk breekt.
Hier is een eenvoudige analogie: Stel je een stapel perfect uitgelijnde knikkers voor. Als je de stapel vanaf de zijkant duwt, verschuiven de knikkers en zakt de stapel gemakkelijk in. Op dezelfde manier zullen ionische verbindingen, met hun dicht opeengepakte ionen, breken in plaats van buigen.
Uitzonderingen: Sommige ionische verbindingen kunnen enige mate van flexibiliteit vertonen als gevolg van factoren zoals:
* Grotere ionische grootte: Grotere ionen hebben zwakkere elektrostatische krachten en kunnen een zekere mate van flexibiliteit mogelijk maken.
* Aanwezigheid van covalente bindingen: Sommige ionische verbindingen kunnen covalente bindingen in hun structuur hebben, wat hun flexibiliteit vergroot.
Samengevat: De brosheid van ionische verbindingen is een direct gevolg van hun sterke elektrostatische krachten en de starre, vaste posities van hun ionen.
 Wat heeft een hoger kookpunt NaCl of CL2?
Wat heeft een hoger kookpunt NaCl of CL2?  Wetenschappers ontwikkelen eerste medicijnachtige verbindingen om ongrijpbare, aan kanker gerelateerde enzymen te remmen
Wetenschappers ontwikkelen eerste medicijnachtige verbindingen om ongrijpbare, aan kanker gerelateerde enzymen te remmen Is de telefoonontvanger een ionische of covalente verbinding?
Is de telefoonontvanger een ionische of covalente verbinding?  Wat zijn enkele voorbeelden van vaste vloeibare oplossingen?
Wat zijn enkele voorbeelden van vaste vloeibare oplossingen?  Essentiële instrumenten voor nauwkeurige luchtdrukmeting
Essentiële instrumenten voor nauwkeurige luchtdrukmeting
 Luchtkwaliteit en gezondheid in de VS zullen verbeteren door acties van andere landen om klimaatverandering te vertragen
Luchtkwaliteit en gezondheid in de VS zullen verbeteren door acties van andere landen om klimaatverandering te vertragen Wat zijn de twee continenten zonder regenwouden?
Wat zijn de twee continenten zonder regenwouden?  Princeton-geologen lossen fossielenmysterie op door een virtuele 3D-tour door rots te maken
Princeton-geologen lossen fossielenmysterie op door een virtuele 3D-tour door rots te maken Gezamenlijk onderzoek richt zich op de noodzaak voor het behoud van bronnen in een droog klimaat
Gezamenlijk onderzoek richt zich op de noodzaak voor het behoud van bronnen in een droog klimaat Terwijl Ian op weg is naar Florida, zetten bewoners zich schrap voor orkaanhel
Terwijl Ian op weg is naar Florida, zetten bewoners zich schrap voor orkaanhel
Hoofdlijnen
- Bacteriën die een plasmide bevatten waarin het eukaryotische gen is geïntegreerd, zouden waar groeien?
- Hoe is het mogelijk dat minder dan 1 procent van de bacteriën ziekte veroorzaken?
- Wie is verantwoordelijk voor het ontwikkelen van de evolutietheorie?
- Waarom apen zieke leden van hun troep aanvallen en geen sociale afstand nemen
- Waarom is de structuur belangrijk voor functie in celmembraan?
- Hoe reizen cellen door ons lichaam?
- Hoe gaan cellen om met osmose?
- Met welke genetische processen kan een soort in de loop van de tijd veranderen?
- Een nieuwe studie toont aan dat mieren voor de verstandigere optie kiezen, zelfs als dat betekent dat je wat harder moet werken
- Chemici bedenken nieuwe Lewis-zuurtest met behulp van fluorescentie

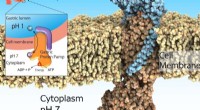
- Onderzoekers stellen kristalstructuur van maagprotonpomp vast
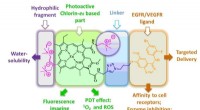
- Nieuwe zeer selectieve antitumor fotodynamische therapiemiddelen gesynthetiseerd
- Onderzoek naar een thermische uitdaging voor MOF's

- Alles samenvoegen:inspiratie voor taaie en zelfherstellende materialen
 Wat zijn de kenmerken van de bodem in gematigde regenwoudbiomen?
Wat zijn de kenmerken van de bodem in gematigde regenwoudbiomen?  Potentiële gendervooroordelen tegen vrouwelijke onderzoekers bij peer review van onderzoeksbeurzen
Potentiële gendervooroordelen tegen vrouwelijke onderzoekers bij peer review van onderzoeksbeurzen Waar staat SBBR3 voor en is het covalent of ionisch?
Waar staat SBBR3 voor en is het covalent of ionisch?  Over de aroma's van wijn piekeren
Over de aroma's van wijn piekeren Wat is oppervlaktezwaartekracht?
Wat is oppervlaktezwaartekracht?  Het energiemechanisme dat wordt gebruikt in het tweede uur van het runnen van een marathon?
Het energiemechanisme dat wordt gebruikt in het tweede uur van het runnen van een marathon?  Onthul de geheimen van plantgezondheid en koolstofopslag met rhizosphere-on-a-chip
Onthul de geheimen van plantgezondheid en koolstofopslag met rhizosphere-on-a-chip Hoe inheemse graslanden in het binnenland van de Pacific Northwest te herstellen
Hoe inheemse graslanden in het binnenland van de Pacific Northwest te herstellen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

