
Wetenschap
Impact van pH op reactiesnelheid:factoren en overwegingen
* pH en reactiesnelheid: De verandering in pH kan de snelheid van een reactie aanzienlijk beïnvloeden, maar de omvang van deze verandering hangt af van de specifieke reactie en het betrokken mechanisme.
* Katalysatoren en pH: Veel reacties worden gekatalyseerd door enzymen of andere moleculen. De activiteit van deze katalysatoren is vaak zeer gevoelig voor de pH.
* Reactiemechanisme: Het specifieke mechanisme van de reactie bepaalt hoe de pH de snelheid beïnvloedt. Bijvoorbeeld:
* Zuurgekatalyseerde reacties: Reacties waarbij een protonenoverdrachtsstap betrokken is, zullen vaak versnellen bij lagere pH-waarden (hogere H+-concentratie).
* Basis-gekatalyseerde reacties: Reacties waarvoor een hydroxide-ion (OH-) nodig is, zullen versnellen bij hogere pH-waarden.
Om te bepalen met welke factor het tarief verandert, moet u het volgende weten:
1. De specifieke reactie: Welke moleculen reageren?
2. Het reactiemechanisme: Welke stappen zijn betrokken bij de reactie?
3. De pH-afhankelijkheid van de snelheidsconstante: Hoe verandert de snelheidsconstante met de pH?
Voorbeeld:
Laten we zeggen dat de reactie een eenvoudige, door zuur gekatalyseerde hydrolyse van een ester is. De snelheidsconstante (k) zou als volgt een relatie kunnen hebben met de pH:
k =k0 * [H+], waarbij k0 een constante is.
In dit geval, als de pH verandert van 6,50 naar 2,00, neemt de [H+] toe met een factor 10^(6,5-2) =10^4,5. Daarom zou de reactiesnelheid toenemen met een factor 10^4,5 .
Zonder meer informatie over de reactie is het onmogelijk om een definitief antwoord te geven over de veranderingsfactor in de snelheid.
 Onderzoeksteam bereikt doorbraak in productie van veelgeprezen kankerbestrijdend medicijn
Onderzoeksteam bereikt doorbraak in productie van veelgeprezen kankerbestrijdend medicijn Hoeveel moleculen koolstoftetrachloride zitten er in 6,32 mg van deze verbinding?
Hoeveel moleculen koolstoftetrachloride zitten er in 6,32 mg van deze verbinding?  Is pH 4 sterker dan ph3?
Is pH 4 sterker dan ph3?  Duurzaam, zeer selectieve biokatalytische omzetting van aldehyden in carbonzuren
Duurzaam, zeer selectieve biokatalytische omzetting van aldehyden in carbonzuren Water is een deel zuurstof en hoeveel delen waterstof?
Water is een deel zuurstof en hoeveel delen waterstof?
 Loodhoudend water:hoe huizen te houden, scholen, kinderdagverblijven en werkplekken veilig
Loodhoudend water:hoe huizen te houden, scholen, kinderdagverblijven en werkplekken veilig De uraniummijn in het hart van Kakadu heeft een beter opruimplan nodig
De uraniummijn in het hart van Kakadu heeft een beter opruimplan nodig Hoe is het landschap van de aarde?
Hoe is het landschap van de aarde?  Koeien maskers? Agrarisch bedrijf probeert methaanabsorberend draagbaar apparaat
Koeien maskers? Agrarisch bedrijf probeert methaanabsorberend draagbaar apparaat Waarom smelten de gletsjers in Zuidoost-Tibet zo snel?
Waarom smelten de gletsjers in Zuidoost-Tibet zo snel?
Hoofdlijnen
- Wat is de naam van het mechanisme dat betrokken is bij het normaal houden van lichaamssystemen?
- Hebben rivieren de evolutie van Sumatraanse cascadekikkers beïnvloed?
- Wat is de betekenis van morfogenese?
- Wat is het deel van de plant dat zijn steun biedt?
- Wie zijn de verschillende biologen en hun bijdragen aan de ontwikkeling van de biologische biotechnologie?
- Identificeer het koninkrijk een eencellig eukaryotisch organisme dat zijn eigen voedsel maakt, behoort tot?
- Begrijpen hoe het COVID-19-virus het lichaam binnendringt en medicijnen die de infectie kunnen verzachten
- Hoe geel en blauw groen maken bij papegaaien
- Wat is het macromolecuul van sprite?
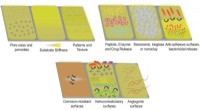
- Op polymeer gebaseerde coatings op metalen implantaten verbeteren de integratie van bot-implantaten
- Hondenvoer verrukkelijker maken door aroma's te analyseren

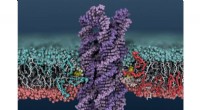
- DNA-enzym schudt celmembranen duizend keer sneller dan zijn natuurlijke tegenhanger
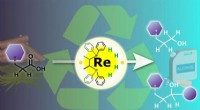
- Chemici zetten metaalkatalyse op zijn kop voor een duurzame toekomst
- Sneller giftige kankerverwekkende metalen vinden in voedsel en water

 Welke rol speelt fysiek verwering in het vormingsproces van zandsteen?
Welke rol speelt fysiek verwering in het vormingsproces van zandsteen?  Onderzoekers onthullen de sleutel tot hoe bacteriën kwikvervuiling opruimen
Onderzoekers onthullen de sleutel tot hoe bacteriën kwikvervuiling opruimen  Wat is het product van Eugenol en Fecl3?
Wat is het product van Eugenol en Fecl3?  Waarom vangt de aardmosfeer energie van de zon?
Waarom vangt de aardmosfeer energie van de zon?  Werkzoekenden vertellen hoeveel andere mensen hebben gesolliciteerd, verhoogt het aantal sollicitaties, diversiteit kan stimuleren
Werkzoekenden vertellen hoeveel andere mensen hebben gesolliciteerd, verhoogt het aantal sollicitaties, diversiteit kan stimuleren Wetenschappers demonstreren met hoge resolutie dat lidar de geboortezone van wolkendruppeltjes ziet, een allereerste observatie op afstand
Wetenschappers demonstreren met hoge resolutie dat lidar de geboortezone van wolkendruppeltjes ziet, een allereerste observatie op afstand  Dating -techniek waarbij fossielen in rotslagen zijn betrokken?
Dating -techniek waarbij fossielen in rotslagen zijn betrokken?  Krachtige nieuwe magneet geeft nieuw inzicht in bevroren kwantummaterialen
Krachtige nieuwe magneet geeft nieuw inzicht in bevroren kwantummaterialen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

