
Wetenschap
Magnesium en zwavel:de vorming van een ionische binding begrijpen
* Elektro-negativiteitsverschil: Magnesium heeft een lage elektronegativiteit (1,31), terwijl zwavel een hogere elektronegativiteit heeft (2,58). Dit significante verschil in elektronegativiteit (1,27) duidt op een sterke neiging van zwavel om elektronen uit magnesium aan te trekken.
* Elektronenconfiguratie:
* Magnesium (Mg) heeft twee valentie-elektronen in de buitenste schil. Het verliest deze twee elektronen gemakkelijk om een stabiele octetconfiguratie te bereiken, zoals het edelgasneon (Ne).
* Zwavel (S) heeft zes valentie-elektronen. Er zijn nog twee elektronen nodig om een stabiele octetconfiguratie te bereiken, zoals het edelgas argon (Ar).
* Vorming van ionen:
* Magnesium verliest zijn twee valentie-elektronen en wordt een positief geladen ion (Mg²⁺).
* Zwavel krijgt twee elektronen en wordt een negatief geladen ion (S²⁻).
* Elektrostatische aantrekkingskracht:
* De tegengesteld geladen ionen (Mg²⁺ en S²⁻) trekken elkaar aan door elektrostatische krachten, waardoor een ionische binding ontstaat.
Het resultaat:
De sterke elektrostatische aantrekkingskracht tussen de positief geladen magnesiumionen (Mg²⁺) en de negatief geladen sulfide-ionen (S²⁻) resulteert in de vorming van een ionische verbinding, magnesiumsulfide (MgS).
 Hoe gezond zijn de Amerikaanse kusten?
Hoe gezond zijn de Amerikaanse kusten?  In uitgebrande bosjes met gigantische sequoia's planten bemanningen hoop; zullen ze overleven?
In uitgebrande bosjes met gigantische sequoia's planten bemanningen hoop; zullen ze overleven?  Wat zijn enkele manieren waarop mensen omgaan met de aarde?
Wat zijn enkele manieren waarop mensen omgaan met de aarde?  De watervoorziening van LA is in goede staat:maar is de stad klaar voor de volgende droogte?
De watervoorziening van LA is in goede staat:maar is de stad klaar voor de volgende droogte?  Bij het bekijken van een object door het krachtige doelstelling van een microscoop kan niet alle obJegect in focus zijn waarom?
Bij het bekijken van een object door het krachtige doelstelling van een microscoop kan niet alle obJegect in focus zijn waarom?
Hoofdlijnen
- Hoe verschillen splitsing en embryo in betekenis?
- Wat is het doel om verschillende celtypen in het lichaam te hebben?
- Wat bepaalt de primaire functie van een eiwit?
- Welk type omgeving functioneren cellen het beste?
- Beschrijf het proces waarmee een schimmel zich voedt?
- Wat is de cellulaire structuur die cytoplasma scheidt van de externe omgeving?
- Wat is wanneer meer cellen worden gemaakt dan sterven?
- Welke soorten organismen kunnen groeien op Endo Agar?
- Wat wordt er gevonden in de plantencellen die chlorofyl bevatten?
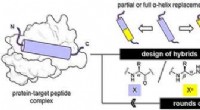
- Oligourea-foldamers bootsen peptiden alfa-helices na en binden effectief aan medicijndoelen
- Wetenschappers lossen ruwe olie op in water om de samenstelling ervan te bestuderen

- Onderzoekers boeken belangrijke vooruitgang in de richting van productie van belangrijke biobrandstof

- Steenkool onthult een verfijnde kant:vuile koolstof kan worden gebruikt om een verscheidenheid aan nuttige apparaten te maken

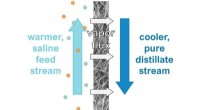
- Hoe maak je zout water beter schoon? Door ontziltingsgereedschappen droog te houden
 Heb je het gezien? Supermoon siert de hemel over de hele wereld
Heb je het gezien? Supermoon siert de hemel over de hele wereld  Wat is de drijvende kracht die op een object werkt?
Wat is de drijvende kracht die op een object werkt?  Nanodeeltjes vormen onder druk superkristallen
Nanodeeltjes vormen onder druk superkristallen Bewijs gevonden van aardbevingen met lage slip die de voortgang van grote destructieve aardbevingen belemmeren
Bewijs gevonden van aardbevingen met lage slip die de voortgang van grote destructieve aardbevingen belemmeren Zijn water en chloor beide voorbeelden van moleculen?
Zijn water en chloor beide voorbeelden van moleculen?  Hoe meet je de afstand in de ruimte en welke methoden worden gebruikt om de enorme afstanden tussen hemelobjecten te bepalen?
Hoe meet je de afstand in de ruimte en welke methoden worden gebruikt om de enorme afstanden tussen hemelobjecten te bepalen?  Hoeveel is de natuur waard?
Hoeveel is de natuur waard?  Denk je dat je griep hebt? De app voor thuisartsconsultatie kan helpen
Denk je dat je griep hebt? De app voor thuisartsconsultatie kan helpen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

