
Wetenschap
Ionische geleidbaarheid:elektrisch gedrag in vaste stoffen en gesmolten toestanden begrijpen
Ionische verbindingen:een herinnering
* Structuur: Ionische verbindingen worden gevormd door de elektrostatische aantrekking tussen positief geladen ionen (kationen) en negatief geladen ionen (anionen). Ze vormen een stijve, kristallijne roosterstructuur.
* Elektronen: Elektronen in ionische verbindingen zijn stevig gebonden aan de ionen en kunnen niet vrij bewegen.
Waarom vaste stoffen niet geleiden
* Vaste posities: In de vaste toestand zijn ionen opgesloten in een vaste roosterstructuur. Ze kunnen zich niet vrij bewegen.
* Gratis vervoerders: Omdat de elektronen aan de ionen gebonden zijn, zijn er geen vrije ladingsdragers die een elektrische stroom kunnen transporteren.
Waarom Molten State optreedt
* Mobiliteit: Wanneer een ionische verbinding smelt, worden de sterke elektrostatische krachten die de ionen bij elkaar houden zwakker. De ionen worden mobiel en kunnen vrij bewegen.
* Kostendragers: De mobiele ionen, die hun positieve of negatieve ladingen dragen, fungeren als ladingsdragers. Wanneer een elektrische potentiaal wordt aangelegd, bewegen deze ionen zich naar de tegengesteld geladen elektrode, waardoor een elektrische stroom ontstaat.
Analogie
Stel je een overvolle kamer voor vol met mensen (ionen) die allemaal dicht op elkaar zitten en niet kunnen bewegen (solid state). Stel je nu voor dat diezelfde mensen zich allemaal vrij rondbewegen (gesmolten toestand). Als je een boodschap door de kamer wilt krijgen, is dat veel gemakkelijker als er mensen in beweging zijn!
Belangrijkste afhaalmaaltijden: De elektrische geleidbaarheid van ionische stoffen is afhankelijk van de mobiliteit van ionen. In de vaste toestand zijn ze gefixeerd, terwijl ze in de gesmolten toestand vrij zijn om te bewegen en lading te dragen.
Hoofdlijnen
- Alpaca's bleken het enige zoogdier te zijn dat rechtstreeks de baarmoeder insemineerde
- Sequentiebepaling van het genoom van stevia-planten voor het eerst onthuld
- Vergelijking van de ademhalingssystemen van kikkers en mensen:belangrijkste overeenkomsten en verschillen
- Wat is het anaërobe metabolisme?
- Een zeldzame epische reis van zangvogels vanaf de rand van uitsterven terug naar de LA River
- Honingbijen ultra-verbonden door hun microbioom
- Hoe communiceren bacteriën?
- Voordelen en nadelen van mitose bij meercellig organisme?
- Welke generatie ondergaat mitose in de sporische levenscyclus?
- Vloeistofachtige beweging in kristallen zou hun veelbelovende gedrag in zonnecellen kunnen verklaren

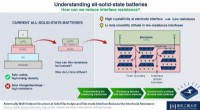
- Glashelder maken:kristalliniteit vermindert de weerstand in volledig solid-state batterijen
- Lab-on-a-disc-technologie belooft te versnellen, DNA-analyse ter plaatse vereenvoudigen

- Een magnesiumchloride-oplossing van 10% bereiden:stapsgewijze instructies

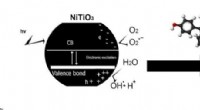
- Chemici zetten titanium nanodeeltjes om in een efficiënt wapen tegen vervuiling
 Actinium (III) Oxide Molecuulformule:Berekening en uitleg
Actinium (III) Oxide Molecuulformule:Berekening en uitleg  Wetenschappers boren voor het eerst op afgelegen Antarctische gletsjer
Wetenschappers boren voor het eerst op afgelegen Antarctische gletsjer Veilig voelen? Probeer een internetbeveiligingsconferentie bij te wonen
Veilig voelen? Probeer een internetbeveiligingsconferentie bij te wonen  Hackers zoeken losgeld uit Baltimore en gemeenschappen in de VS
Hackers zoeken losgeld uit Baltimore en gemeenschappen in de VS De hoeveelheid water in een beker neemt af, is dit een voorbeeldevenwicht?
De hoeveelheid water in een beker neemt af, is dit een voorbeeldevenwicht?  De psychologie van rellen:waarom het nooit zomaar zinloos geweld is?
De psychologie van rellen:waarom het nooit zomaar zinloos geweld is? Heeft onze zon buitenaardse werelden veroverd?
Heeft onze zon buitenaardse werelden veroverd?  XY-coördinaten converteren naar lengtegraad en breedtegraad
XY-coördinaten converteren naar lengtegraad en breedtegraad
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


