
Wetenschap
Ionische verbindingen:elektrische geleidbaarheid in vaste en gesmolten toestanden
Dit is waarom:
* Ionische verbindingen: Deze verbindingen worden gevormd door de elektrostatische aantrekking tussen positief geladen ionen (kationen) en negatief geladen ionen (anionen).
* Solid State: In de vaste toestand worden de ionen stevig vastgehouden in een kristalroosterstructuur. Deze vaste opstelling verhindert de vrije beweging van ionen, en dus geen elektrische geleiding.
* Gesmolten staat: Wanneer ze gesmolten zijn, breken de ionen los van de roosterstructuur en worden ze mobiel. Hierdoor kunnen ze elektrische lading dragen, wat resulteert in geleidbaarheid.
Voorbeeld: Natriumchloride (NaCl) is een veel voorkomende ionische verbinding. In vaste vorm (keukenzout) geleidt het geen elektriciteit, maar gesmolten geleidt het wel goed.
 Rogge voor de gelegenheid:onderzoeken hoe winterroggevariëteiten geschikt zijn voor verschillende klimaten
Rogge voor de gelegenheid:onderzoeken hoe winterroggevariëteiten geschikt zijn voor verschillende klimaten  Studie van pekelafvoer uit ontziltingsinstallatie vindt goed nieuws en slecht nieuws
Studie van pekelafvoer uit ontziltingsinstallatie vindt goed nieuws en slecht nieuws De snelle opwarming van het noordpoolgebied heeft in het verleden de winden van de Zuidelijke Oceaan verschoven
De snelle opwarming van het noordpoolgebied heeft in het verleden de winden van de Zuidelijke Oceaan verschoven Eetbare wilde planten in New Hampshire
Eetbare wilde planten in New Hampshire Waarom werd orkaan Patricia zo snel een monster?
Waarom werd orkaan Patricia zo snel een monster?
Hoofdlijnen
- Schadelijke genen:waarom schadelijke varianten blijven bestaan in menselijke populaties
- Wat doet een cel overdag?
- Hoe gaat water in en uit een cel?
- Wat is trobologie?
- Extreme zoutstress veroorzaakt bladbeweging
- Welk gewricht is een voorbeeld van syndesmose?
- Welk doel dienen de antilichamen in het bloed?
- Wat is een organisme dat zijn energie verkrijgt van het voedsel dat het eet?
- Welke soorten bewijs gebruiken wetenschappers om een organisme op een fylogene boom te plaatsen en wat vertelt die plaats je?
- Moleculen gevonden in slijm kunnen schimmelinfecties tegengaan
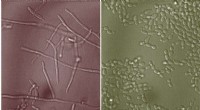
- Alcohol omzetten in belangrijke ingrediënten voor nieuwe medicijnen

- Onderzoekers onderzoeken ontstekingsremmende activiteit van curcumine

- Nieuw nano-apparaat zou zonne-energie kunnen gebruiken om waterstof te produceren
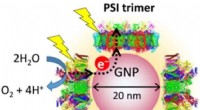
- Wetenschappers melden remming van cellulaire veroudering
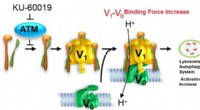
 orkanen, zware regenval is van cruciaal belang voor de grondwatervoorziening van Hawaï
orkanen, zware regenval is van cruciaal belang voor de grondwatervoorziening van Hawaï Het ontwikkelen van een symbiotische relatie tussen E. coli en stinkwantsen onthult aanwijzingen over hoe symbiose zich ontwikkelt
Het ontwikkelen van een symbiotische relatie tussen E. coli en stinkwantsen onthult aanwijzingen over hoe symbiose zich ontwikkelt  Vertragingen in landgebruik kunnen klimaatinspanningen belemmeren
Vertragingen in landgebruik kunnen klimaatinspanningen belemmeren Is het buigen van koper een fysiek van chemische verandering?
Is het buigen van koper een fysiek van chemische verandering?  Toename van broeikasgassen, de uitstoot van fijnstof zorgt voor regionale droging over de hele wereld
Toename van broeikasgassen, de uitstoot van fijnstof zorgt voor regionale droging over de hele wereld Welke drie processen transfom metamorfe en sedimentaire rotsen in sediment?
Welke drie processen transfom metamorfe en sedimentaire rotsen in sediment?  Was er ooit een zonne -flare?
Was er ooit een zonne -flare?  Studie zegt dat 2035 klimaatverandering een punt van geen terugkeer is
Studie zegt dat 2035 klimaatverandering een punt van geen terugkeer is
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

