
Wetenschap
Ionische geleidbaarheid en ionengrootte:een gedetailleerde uitleg
1. Mobiliteit:
* Kleinere ionen zijn over het algemeen mobieler: Kleinere ionen ervaren minder wrijving met de omringende oplosmiddelmoleculen of kristalrooster. Hierdoor kunnen ze gemakkelijker door het medium bewegen, waardoor de geleidbaarheid toeneemt.
* Grotere ionen ervaren een grotere weerstand: Grotere ionen hebben een groter oppervlak, wat leidt tot een grotere interactie met de omgeving, waardoor de weerstand toeneemt en de mobiliteit wordt verminderd.
2. Hydratatie:
* Kleinere ionen hebben hogere hydratatiegetallen: Ze hebben een hogere ladingsdichtheid, trekken meer oplosmiddelmoleculen aan (zoals water) en vormen een hydratatieschil eromheen. Deze schaal vergroot de effectieve grootte van het ion, waardoor de beweging ervan wordt belemmerd.
* Grotere ionen hebben lagere hydratatiegetallen: Ze hebben een lagere ladingsdichtheid en trekken minder oplosmiddelmoleculen aan. Dit leidt tot een kleinere hydratatieschil en potentieel grotere mobiliteit.
* Dit is echter niet altijd het geval: Het hydratatiegetal kan aanzienlijk worden beïnvloed door de lading van het ion, en soms kunnen grotere ionen hogere hydratatiegetallen hebben.
3. Roosterstructuur (in vaste stoffen):
* Kleinere ionen passen beter in het kristalrooster: In ionische vaste stoffen kunnen kleinere ionen gemakkelijker ruimtes in het kristalrooster innemen. Dit zorgt voor een grotere ionenmigratie en een verhoogde geleidbaarheid.
* Grotere ionen verstoren het rooster: Grote ionen kunnen de reguliere structuur van het rooster verstoren, wat leidt tot een lagere geleidbaarheid.
4. Concentratie:
* Hoge concentraties kunnen de geleidbaarheid verminderen: Hoewel het contra-intuïtief lijkt, kunnen ionen bij hoge concentraties elkaars beweging verstoren, waardoor de algehele geleidbaarheid wordt verminderd. Dit komt door verhoogde ion-ion-interacties.
5. Temperatuur:
* Verhoogde temperatuur verbetert over het algemeen de geleidbaarheid: Bij hogere temperaturen hebben de ionen meer kinetische energie, waardoor ze vrijer kunnen bewegen en de barrières voor hun beweging kunnen overwinnen.
Samengevat:
Hoewel een kleiner formaat zich doorgaans vertaalt in een hogere mobiliteit en een betere ionische geleidbaarheid, is de invloed van de ionengrootte op de geleidbaarheid niet eenvoudig. Het is een complex samenspel van verschillende factoren, waaronder hydratatie, roosterstructuur, concentratie en temperatuur.
Voorbeelden:
* Lithium-ionbatterijen: Lithiumionen zijn klein en zeer mobiel, waardoor ze ideaal zijn voor gebruik in batterijen.
* Natrium-ionbatterijen: Natriumionen zijn groter dan lithiumionen, maar ze zijn nog steeds relatief mobiel en kunnen in batterijen worden gebruikt.
* Magnesium-ionbatterijen: Magnesiumionen zijn zelfs groter dan natriumionen, waardoor ze minder mobiel zijn en tot een lagere geleidbaarheid leiden.
Daarom is het van cruciaal belang om al deze factoren in overweging te nemen bij het ontwerpen van materialen voor specifieke toepassingen die afhankelijk zijn van ionische geleidbaarheid.
 Wat is de chemische formule van waterstofchloraat?
Wat is de chemische formule van waterstofchloraat?  Welk mineraal heeft een perfecte splitsing in zes richtingen:diamantfluoriet, sodaliet en sfaleriet?
Welk mineraal heeft een perfecte splitsing in zes richtingen:diamantfluoriet, sodaliet en sfaleriet?  Is bijtende frisdrank uit een natuurlijke bron?
Is bijtende frisdrank uit een natuurlijke bron?  Wat gebeurt er hoogstwaarschijnlijk met de reactiesnelheid van een menselijk enzym als de temperatuur geleidelijk wordt verhoogd van 10 graden Celsius naar 30 graden Celsius?
Wat gebeurt er hoogstwaarschijnlijk met de reactiesnelheid van een menselijk enzym als de temperatuur geleidelijk wordt verhoogd van 10 graden Celsius naar 30 graden Celsius?  Welke planten veranderen van kleur vanwege de pH?
Welke planten veranderen van kleur vanwege de pH?
Hoofdlijnen
- Wat verklaart het beste waarom DNA -technologie belangrijk is voor ziektepreventie?
- Orgelsystemen betrokken bij homeostase
- Waarom zijn mensen geen 'knokkellopers'?
- Hoe is een nauwe relatie tussen twee soorten die worden genoemd?
- Hoe weten wetenschappers dat levende wezens gerelateerd zijn?
- Onderzoek werpt nieuw licht op de soortoverschrijdende virusoverloop die pandemieën kan veroorzaken
- Hoe een 'dirigent' betekenis geeft aan chaos in vroege muizenembryo's
- Het Vomeronasale orgel:een rudimentaire structuur die bij sommige mensen aanwezig is
- De polaire kop van een fosfolipide wordt gemaakt welke moleculen?
- Een alternatieve route voor het bestuderen van de intrinsieke eigenschappen van vastestofmaterialen

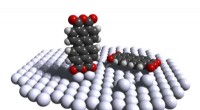
- Lastige prestatie met opstaand molecuul
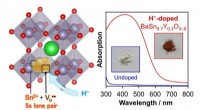
- Succesvolle synthese van perovskiet zichtbaar lichtabsorberend halfgeleidermateriaal
- Vrijstaande microwire-array maakt flexibel zonnevenster mogelijk

- Chemici leren hoe ze fenolen in gerookte voedselmonsters kunnen detecteren met behulp van vitamine B4

 Vacatures kristaldefecten sleutel tot verbeterd ontwerp van lichtgewicht aluminiumlegeringen
Vacatures kristaldefecten sleutel tot verbeterd ontwerp van lichtgewicht aluminiumlegeringen metallische waterstof, eenmaal theorie, wordt werkelijkheid
metallische waterstof, eenmaal theorie, wordt werkelijkheid Welke elementen vormen gewoonlijk meerdere ionen? Overgangsmetalen begrijpen
Welke elementen vormen gewoonlijk meerdere ionen? Overgangsmetalen begrijpen  Wat is de chemische reactie tussen waterstofbromide en water?
Wat is de chemische reactie tussen waterstofbromide en water?  Wat is de hoogste vorm van land op het oppervlak?
Wat is de hoogste vorm van land op het oppervlak?  Foto-responsieve eiwithydrogels als middel voor gecontroleerde afgifte van stamcellen/eiwitten
Foto-responsieve eiwithydrogels als middel voor gecontroleerde afgifte van stamcellen/eiwitten Effect van versnelling als gevolg van zwaartekracht?
Effect van versnelling als gevolg van zwaartekracht?  Hoeveel protonen heeft een atoom van Co-60?
Hoeveel protonen heeft een atoom van Co-60?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

