
Wetenschap
Ozon (O3):moleculaire polariteit en binding begrijpen
* Moleculaire geometrie: Ozon heeft een gebogen moleculaire geometrie. Dit betekent dat de drie zuurstofatomen niet in een rechte lijn zijn gerangschikt, waardoor een ongelijkmatige verdeling van de elektronendichtheid ontstaat.
* Polaire obligaties: Elke zuurstof-zuurstofbinding in ozon is een polaire covalente binding. Dit komt omdat zuurstof elektronegatiever is dan de andere zuurstofatomen, waardoor de gedeelde elektronen dichter naar zichzelf toe worden getrokken.
* Symmetrie: Ondanks de polaire bindingen is het molecuul symmetrisch. De individuele bindingsdipolen heffen elkaar op, wat resulteert in een netto dipoolmoment van nul .
Ook al heeft ozon polaire bindingen, de symmetrische vorm maakt het dus tot een niet-polair molecuul.
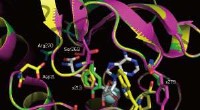
 In vitro/in silico-evaluaties van bindingsaffiniteiten van perfluoralkylstoffen aan Baikal-afdichting PPARα
In vitro/in silico-evaluaties van bindingsaffiniteiten van perfluoralkylstoffen aan Baikal-afdichting PPARα EU-programma ontdekt grootste ozongat in jaren boven Antarctica
EU-programma ontdekt grootste ozongat in jaren boven Antarctica Zijn mist en mist hetzelfde?
Zijn mist en mist hetzelfde?  De dode zone van de Golf van Mexico is al een ramp, maar het kan nog erger worden
De dode zone van de Golf van Mexico is al een ramp, maar het kan nog erger worden NASA bereidt zich voor op nieuwe wetenschappelijke vluchten boven de kust van Louisiana
NASA bereidt zich voor op nieuwe wetenschappelijke vluchten boven de kust van Louisiana
Hoofdlijnen
- Wat zijn agnostische spierparen?
- Hoe DNA wordt vernietigd door virus?
- Wat doen zowel zaden als planten voordat ze beginnen te groeien?
- Landbouwfungicide trekt honingbijen aan, studie vondsten
- Waar worden stamcellen in het lichaam bewaard?
- Wat is de belangrijkste verbinding in DNA?
- Wat is de functie van eenvoudig kolomvormig epitheel?
- Welk deel van de ademhaling produceert de meeste ATP?
- Wat is de naam voor een dun type pincet die in een wetenschappelijk laboratorium wordt gebruikt?
- Ag3PO4-katalysator vergemakkelijkt de elektro-oxidatie van propyleenoxide

- Gerichte evolutie om enzymen te ontwerpen die beeldvormende middelen maken voor medische diagnose
- Modern poreus materiaal lijkt op XIV-eeuws Alhambra-mozaïek

- PEF daagt PET uit voor de strijd

- Een belangrijke aanvulling op de toolkit voor scheikundigen voor het bouwen van nieuwe moleculen

 Wat voor soort sediment bestaat voornamelijk minerale korrels die geërodeerde rotsen op het land waren geërodeerd?
Wat voor soort sediment bestaat voornamelijk minerale korrels die geërodeerde rotsen op het land waren geërodeerd?  Wat is het gewicht van een ruimteraket?
Wat is het gewicht van een ruimteraket?  Video:Brengen menselijke begrafenispraktijken de ecosystemen van de aarde in de war?
Video:Brengen menselijke begrafenispraktijken de ecosystemen van de aarde in de war? Als de aarde van west naar oost roteert, waarom gaan zon en sterren naar het westen?
Als de aarde van west naar oost roteert, waarom gaan zon en sterren naar het westen?  Een gebruik van thermische expansie in gassen geven?
Een gebruik van thermische expansie in gassen geven?  Waar zou een hoofdreeksster die cooler en dimmer is dan de zon in de grafiek verschijnen?
Waar zou een hoofdreeksster die cooler en dimmer is dan de zon in de grafiek verschijnen?  Geslagen energie in welke vorm dan ook wordt aangeduid als wat voor soort energie?
Geslagen energie in welke vorm dan ook wordt aangeduid als wat voor soort energie?  Hoe India's 'krottenwijkvrije' herontwikkeling de bewoners in de steek laat door hun ontwerpinzichten en -behoeften te negeren
Hoe India's 'krottenwijkvrije' herontwikkeling de bewoners in de steek laat door hun ontwerpinzichten en -behoeften te negeren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

