
Wetenschap
Dissociatie van elektrolyten in water:het proces begrijpen
1. Dissociatie:
* De ionische bindingen die de elektrolyt bij elkaar houden, breken.
* De individuele ionen (kationen en anionen) worden omringd door watermoleculen en vormen een zogenaamde hydratatieschil.
* Dit proces wordt dissociatie genoemd .
2. Geleidbaarheid:
* De aanwezigheid van vrije ionen in de oplossing zorgt voor de stroom van elektrische stroom.
*Dit is de reden waarom elektrolyten elektriciteit geleiden.
3. Colligatieve eigenschappen:
*De aanwezigheid van opgeloste ionen beïnvloedt de volgende eigenschappen van de oplossing:
* Dampdrukverlaging: De dampspanning van de oplossing neemt af in vergelijking met zuiver water.
* Kookpunthoogte: Het kookpunt van de oplossing neemt toe in vergelijking met zuiver water.
* Vriespuntdaling: Het vriespunt van de oplossing neemt af in vergelijking met zuiver water.
* Osmotische druk: De osmotische druk van de oplossing neemt toe in vergelijking met zuiver water.
4. Chemische reacties:
*De opgeloste ionen kunnen deelnemen aan chemische reacties.
*Dit is belangrijk bij veel biologische processen, zoals zenuwimpulsen en spiersamentrekkingen.
5. pH-veranderingen:
*De toevoeging van elektrolyten kan de pH van de oplossing beïnvloeden.
* Sterke zuren en basen dissociëren bijvoorbeeld volledig in water, wat leidt tot aanzienlijke pH-veranderingen.
Over het geheel genomen resulteert de toevoeging van ionisch gebonden elektrolyten aan water in een oplossing met:
* Verhoogde geleidbaarheid
* Gewijzigde colligatieve eigenschappen
* Potentieel voor chemische reacties
* Mogelijke pH-veranderingen
De specifieke effecten zijn afhankelijk van de aard van de elektrolyt (de sterkte, concentratie en chemische eigenschappen ervan).
 Hoe beïnvloedt concentratie de reactiesnelheid?
Hoe beïnvloedt concentratie de reactiesnelheid?
Verhogen van de concentratie van reactanten verhoogt in het algemeen de reactiesnelheid omdat meer van de reagerende moleculen of ionen aanwezig zijn om de reactieproducten te vormen. Dit is vooral
 Wat is een voorbeeld van synthese?
Wat is een voorbeeld van synthese?  SARS-CoV-2 in vaste stoffen in afvalwater kan de verspreiding van COVID-19 helpen monitoren
SARS-CoV-2 in vaste stoffen in afvalwater kan de verspreiding van COVID-19 helpen monitoren Is de reactie tussen magnesiumnitraat en kaliumchromaat chemisch of fysiek Wat is vergelijking voor deze reactie?
Is de reactie tussen magnesiumnitraat en kaliumchromaat chemisch of fysiek Wat is vergelijking voor deze reactie?  Wat is de Bond-hoekstructuur en -vorm voor propaan?
Wat is de Bond-hoekstructuur en -vorm voor propaan?
 Welk object geeft zijn eigen licht af?
Welk object geeft zijn eigen licht af?  Hoe zijn voedselwebben op land en in water anders?
Hoe zijn voedselwebben op land en in water anders?  Bosbranden domineren in toenemende mate de koolstofemissies in de Amazone tijdens droogtes
Bosbranden domineren in toenemende mate de koolstofemissies in de Amazone tijdens droogtes Wetenschappers stellen bindende doelen voor om Amazon te redden
Wetenschappers stellen bindende doelen voor om Amazon te redden Hoe stille milieuactivisten de biodiversiteit kunnen helpen beschermen
Hoe stille milieuactivisten de biodiversiteit kunnen helpen beschermen
Hoofdlijnen
- Wat is de primaire functie van DNA?
- Door alles te proberen, leert de roofzuchtige zeeslak wat hij niet mag eten
- Hoe het eten van natto de stresstolerantie en een lang leven kan vergroten
- Waar kun je prokaryotische cellen vinden?
- Waar zijn planten en dieren van gemaakt?
- Welke verbinding die is afgeleid van glucose komt daadwerkelijk de Krebs -cyclus binnen?
- Sarcodina Life Cycle
- Wat zijn vijf evolutionaire krachten?
- Welke fase van de celcyclus zijn typecellen in uw lichaam die niet langer mitoses ondergaan?
- Emissies van verhitte tabaksproducten onderzoeken

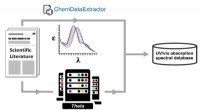
- Automatische aanmaak van databases voor materiaalontdekking:innovatie uit frustratie
- Kunstmatige fotosynthesetechnologie in opkomst

- Er worden nieuwe biologisch afbreekbare polyurethaanschuimen ontwikkeld van tarwestro

- De spanning van een cel meten met een molecuul
 Welk gas wordt opgebruikt en wat wordt er geproduceerd bij de ademhaling?
Welk gas wordt opgebruikt en wat wordt er geproduceerd bij de ademhaling?  Komt biomassa -energie van planten?
Komt biomassa -energie van planten?  De lente komt eerder in de VS, en dat is geen goed nieuws
De lente komt eerder in de VS, en dat is geen goed nieuws Welk proces verplaatst elektronen van het ene object naar het andere door ze tegen elkaar te wrijven?
Welk proces verplaatst elektronen van het ene object naar het andere door ze tegen elkaar te wrijven?  Waarom geeft een micro-organisme uit Yellowstone de voorkeur aan magere rantsoenen boven rijke?
Waarom geeft een micro-organisme uit Yellowstone de voorkeur aan magere rantsoenen boven rijke?  Wetenschappers vinden dat de eeuwige Nijl ouder is dan eerder werd gedacht
Wetenschappers vinden dat de eeuwige Nijl ouder is dan eerder werd gedacht Polyethyleenglycol Vs. Ethyleenglycol
Polyethyleenglycol Vs. Ethyleenglycol  Twee deeltjes van gelijke massa hebben hetzelfde lineaire momentum welke heeft een grotere KE?
Twee deeltjes van gelijke massa hebben hetzelfde lineaire momentum welke heeft een grotere KE?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

