
Wetenschap
Inzicht in de zuurgraad van trichloorazijnzuur (TCA) versus dichloorazijn- en monochloorazijnzuur
Hier is een overzicht van waarom:
* Inductief effect: Chloor is elektronegatiever dan koolstof en waterstof. Dit betekent dat chlooratomen de elektronendichtheid wegtrekken van het koolstofatoom waaraan ze zijn gehecht. Dit elektronenzuigende effect wordt het inductieve effect genoemd.
* Stabilisatie van de geconjugeerde base: Wanneer een carbonzuur een proton (H+) verliest, vormt het een carboxylaatanion (RCOO-). Hoe stabieler de geconjugeerde base, hoe sterker het zuur.
* Trichloorazijnzuur: In trichloorazijnzuur oefenen drie chlooratomen een sterk inductief effect uit op het carboxylaatanion, waardoor de elektronendichtheid wordt onttrokken en de negatieve lading wordt gestabiliseerd. Dit maakt de geconjugeerde base stabieler en het zuur sterker.
* Dichloorazijnzuur: Dichloorazijnzuur heeft twee chlooratomen, wat leidt tot een zwakker inductief effect vergeleken met trichloorazijnzuur. Dit resulteert in een minder stabiele geconjugeerde base en een zwakker zuur.
* Monochloorazijnzuur: Monochloorazijnzuur heeft slechts één chlooratoom, wat resulteert in het zwakste inductieve effect van de drie. Bijgevolg is de geconjugeerde base het minst stabiel, waardoor het het zwakste zuur is.
Samengevat: Hoe meer chlooratomen aanwezig zijn op het azijnzuurmolecuul, hoe sterker het inductieve effect, wat leidt tot een stabielere geconjugeerde base en een sterker zuur.
 Wat is de chemische naam van PT3 (PO3) 4?
Wat is de chemische naam van PT3 (PO3) 4?  Wat betekent halfwaardetijd van uranium 235?
Wat betekent halfwaardetijd van uranium 235?  Vintage wijnen identificeren aan de hand van hun chemische signatuur
Vintage wijnen identificeren aan de hand van hun chemische signatuur  In voor een substantie om wit te lijken, wat moet er alle golflengten van licht gebeuren?
In voor een substantie om wit te lijken, wat moet er alle golflengten van licht gebeuren?  Covalente bindingen en elektrische geleidbaarheid:het verschil begrijpen
Covalente bindingen en elektrische geleidbaarheid:het verschil begrijpen
 Aanpak van het stedelijke hitte-effect in nieuw onderzoeksrapport over het koelen van gemeenschappelijke ruimtes
Aanpak van het stedelijke hitte-effect in nieuw onderzoeksrapport over het koelen van gemeenschappelijke ruimtes Regionale variaties in overconsumptie van zoet water
Regionale variaties in overconsumptie van zoet water De tweejaarlijkse regenrelatie op het tropische westelijk halfrond is de afgelopen decennia verzwakt
De tweejaarlijkse regenrelatie op het tropische westelijk halfrond is de afgelopen decennia verzwakt Sociaal-economisch, milieueffecten van COVID-19 gekwantificeerd
Sociaal-economisch, milieueffecten van COVID-19 gekwantificeerd CO2-sensoren in twee stedelijke gebieden registreerden een grote daling van de uitstoot tijdens de COVID-19-pandemie
CO2-sensoren in twee stedelijke gebieden registreerden een grote daling van de uitstoot tijdens de COVID-19-pandemie
Hoofdlijnen
- Wat is de waarde die u vertelt of S fossiel jonger of ouder is?
- Welk vakgebied wordt geassocieerd met het bestuderen van planten?
- Wat is de definitie van agrigultuur?
- Studeert een arts menselijke cel- of dierlijke cellen?
- Op welke vier manieren kunnen de ziekteverwekkers mensen infecteren?
- In welke tak van de wetenschap is biologisch?
- Hoe fungeren de mitochondriën als keuken van cel?
- Welk type ademhaling presteert spiercellen?
- Waarom is de hypothese zo belangrijk voor de wetenschappelijke methode?
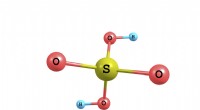
- Berekening van ionenconcentraties in een zwavelzuuroplossing van 0,010 M
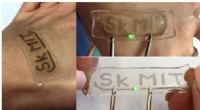
- Team ontwikkelt eenvoudige hydrogel-modificatiemethode voor rekbare en transparante elektronica
- Onderzoekers gebruiken elektrostatische lading om deeltjes te assembleren tot materialen die edelstenen nabootsen, zout

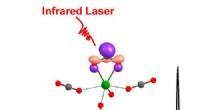
- Wetenschappers identificeren overgangsmetaal voor zeer efficiënte kooldioxide-activering
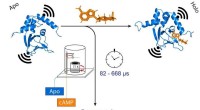
- Onderzoekers onderzoeken structurele veranderingen in snel ingevroren eiwitten
 Zeer efficiënte ammoniaksynthesekatalysator ontwikkeld
Zeer efficiënte ammoniaksynthesekatalysator ontwikkeld Chemici maken nanobuisstructuren die kunnen uitzetten en krimpen zonder af te breken
Chemici maken nanobuisstructuren die kunnen uitzetten en krimpen zonder af te breken Definitie van celoppervlakte-eiwitten
Definitie van celoppervlakte-eiwitten Voordelen en nadelen van Ethanol Biofuel
Voordelen en nadelen van Ethanol Biofuel Onderzoekers ontwikkelen een materiaal dat nabootst hoe de hersenen informatie opslaan
Onderzoekers ontwikkelen een materiaal dat nabootst hoe de hersenen informatie opslaan  Trainen van de trainers:Hoe stress te minimaliseren wanneer paarden voor het eerst worden bereden
Trainen van de trainers:Hoe stress te minimaliseren wanneer paarden voor het eerst worden bereden  Nederlandse realityshow gaat enkele reis Mars aanbieden
Nederlandse realityshow gaat enkele reis Mars aanbieden  Wat gebeurt er met de sterkte van de zwaartekracht wanneer de afstand wordt verdubbeld?
Wat gebeurt er met de sterkte van de zwaartekracht wanneer de afstand wordt verdubbeld?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

