
Wetenschap
Inzicht in de bindingshoek van 92 graden in waterstofsulfide (H₂S)
1. Afstoting van eenzaam paar:
* Zwavel in H₂S heeft naast de twee bindingsparen met waterstofatomen twee vrije elektronenparen.
* Alleenstaande paren nemen meer ruimte in beslag dan bindingsparen vanwege hun hogere elektronendichtheid.
* Deze eenzame paren oefenen sterkere afstotende krachten uit op de bindingsparen, waardoor de waterstofatomen dichter bij elkaar worden gedrukt en de H-S-H-bindingshoek kleiner wordt.
2. Hybridisatie:
* Het zwavelatoom in H₂S is sp³ gehybridiseerd, wat betekent dat het vier orbitalen heeft met gelijke energieniveaus.
*De twee eenzame paren bezetten echter twee van deze orbitalen, waardoor er slechts twee overblijven voor binding met waterstof.
* Deze hybridisatie leidt tot een vervormde tetraëdrische geometrie met een kleinere bindingshoek.
3. Kleinere omvang van waterstofatoom:
* Waterstofatomen zijn erg klein vergeleken met zwavel.
* Door dit kleine formaat kunnen de waterstofatomen dichter bij elkaar zijn, wat verder bijdraagt aan de kleinere bindingshoek.
4. Afwezigheid van sterke intermoleculaire krachten:
* H₂S is een polair molecuul, maar heeft relatief zwakke intermoleculaire krachten vanwege het lage elektronegativiteitsverschil tussen waterstof en zwavel.
* Door dit gebrek aan sterke intermoleculaire krachten kan het molecuul een meer ontspannen conformatie aannemen met een kleinere bindingshoek.
Samenvattend draagt de combinatie van afstoting van een eenzaam paar, sp³-hybridisatie, de kleine omvang van waterstof en zwakke intermoleculaire krachten bij aan de bindingshoek van 92 graden in waterstofsulfide.
 Wat is acetaatpapier?
Wat is acetaatpapier?  Wanneer de warmte van de reactie van de reactie verschuift, is er een verandering in concentratie geweest en wordt het evenwicht vervolgens beïnvloed?
Wanneer de warmte van de reactie van de reactie verschuift, is er een verandering in concentratie geweest en wordt het evenwicht vervolgens beïnvloed?  Science Fair-projecten over Milk & Food Coloring
Science Fair-projecten over Milk & Food Coloring Is roeren suiker in een kopje thee -fysische of chemische verandering?
Is roeren suiker in een kopje thee -fysische of chemische verandering?  Wat voor soort krachten bestaan er tussen zuurstofmoleculen in vloeibare zuurstof?
Wat voor soort krachten bestaan er tussen zuurstofmoleculen in vloeibare zuurstof?
 NASA's Terra Satellite ziet het einde van Bavi
NASA's Terra Satellite ziet het einde van Bavi Door de bomen het bos zien:hoe archeologen hazelnoten gebruiken om oude bossen te reconstrueren
Door de bomen het bos zien:hoe archeologen hazelnoten gebruiken om oude bossen te reconstrueren  De ecologische restauratieprojecten van China putten de watervoorraden op het land uit
De ecologische restauratieprojecten van China putten de watervoorraden op het land uit In Libanon, zoutproducenten vrezen dat ambacht opdroogt
In Libanon, zoutproducenten vrezen dat ambacht opdroogt Water is belangrijk voor levende systemen weerspiegelt?
Water is belangrijk voor levende systemen weerspiegelt?
Hoofdlijnen
- Hebben alle cellen een kopie van het erfelijke materiaal?
- Wat doet de vacuole -organel in een plantencel?
- Welk type transport vereist ATP om moleculen te verplaatsen?
- Wat voor soort structuur produceren verticale hyfen?
- Waar wordt Golgi -apparaten gevonden in een cel?
- Waarom leven dieren in de Dode Zee?
- Wat is een beschrijvingscellen?
- Een ziekte die deeltje veroorzaakt van RNA zonder capside wordt genoemd?
- Hoe beïnvloedt de evolutietheorie van de manier waarop ziekten en behandelingen worden benaderd?
- Activering van koolstof-fluorbindingen door samenwerking van een fotokatalysator en tin

- TNT zou na 116 jaar op pensioen kunnen gaan

- Voedingswetenschappers willen plantaardige eiwitten lekkerder en gezonder maken

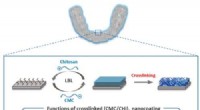
- Tandhouders en aligners helpen om bacteriën te bestrijden
- Hoe atomaire massa-eenheden naar joules om te zetten:een praktische gids

 Welke chemische binding in DNA?
Welke chemische binding in DNA?  Nieuwe aanwijzingen over hoe planten gezonde genomen behouden en mitochondriale ziekten vermijden
Nieuwe aanwijzingen over hoe planten gezonde genomen behouden en mitochondriale ziekten vermijden  300 jaar oud zuigerontwerp opnieuw uitgevonden met zachte flexibele materialen
300 jaar oud zuigerontwerp opnieuw uitgevonden met zachte flexibele materialen Zijn eiwitdierlijke cellen of plantencellen?
Zijn eiwitdierlijke cellen of plantencellen?  Wie won de Nobelprijs in de natuurkunde 1908?
Wie won de Nobelprijs in de natuurkunde 1908?  Gebruik voor gemiddelde, mediaan en modus
Gebruik voor gemiddelde, mediaan en modus Onderzoekers ontwikkelen 's werelds eerste alcoholische drank gemaakt van tofu-wei
Onderzoekers ontwikkelen 's werelds eerste alcoholische drank gemaakt van tofu-wei Hoeveel elektronen op koolstof 14?
Hoeveel elektronen op koolstof 14?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

