
Wetenschap
Berekening van het oxidatiegetal van lood (Pb) in PbH4:een stapsgewijze handleiding
Zo bepaal je het oxidatiegetal van Pb in PbH4:
* Oxidatiegetal van waterstof: Waterstof heeft doorgaans een oxidatiegetal van +1, behalve wanneer het aan een metaal is gebonden, in welk geval het een oxidatiegetal van -1 heeft.
* Totale kosten: PbH4 is een neutraal molecuul, wat betekent dat de totale lading nul is.
Laten we de vergelijking opstellen:
* Laat 'x' het oxidatiegetal van Pb zijn.
* We hebben 4 waterstofatomen, elk met een oxidatiegetal van -1.
Daarom is de vergelijking:x + 4(-1) =0
Oplossing voor x:
* x - 4 =0
* x =+4
Het oxidatiegetal van Pb in PbH4 is +4.
 De eerste weergave van verwering op angströmschaal
De eerste weergave van verwering op angströmschaal Suomi NPP ziet tyfoon Maria Guam . treffen
Suomi NPP ziet tyfoon Maria Guam . treffen De toenemende droogte stelt de veerkracht van het Amazone-regenwoud op de proef
De toenemende droogte stelt de veerkracht van het Amazone-regenwoud op de proef  Langetermijnstudie onthult voordelen voor de volksgezondheid door vermindering van luchtvervuiling
Langetermijnstudie onthult voordelen voor de volksgezondheid door vermindering van luchtvervuiling Alfalfa verlies? Jaarlijks raaigras is een win
Alfalfa verlies? Jaarlijks raaigras is een win
Hoofdlijnen
- Welk deel van een plantencel regelt de activiteiten andere cellen?
- Wetenschappers laten zien hoe vrouwelijke gameten het herstel van de bevruchting in bloeiende planten regelen
- Waar zijn moleculen in het lichaam?
- Vertonen alle bacteriën een vergelijkbaar cultureel kenmerk?
- Uit welke 3 structuren bestaat het buitenoor?
- Nepal op schema om doel van verdubbeling tijgerpopulatie tegen 2022 te halen
- Wat gebeurt er met de meeste organismen als ze sterven?
- Nieuw model helpt verklaren hoe voorzieningen ziekten in het wild bevorderen of verminderen
- Wat is de betekenis van de bifocale wetenschap?
- Onderzoekers gebruiken zink om insulineproducerende cellen aan te vallen met regeneratief medicijn
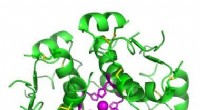
- Van kegelslakkengif tot pijnverlichting

- Onderzoek toont aan dat afzonderlijke atomen efficiëntere katalysatoren kunnen maken

- Team ontwikkelt peptide dat resistente bacteriën weer gevoelig maakt voor antibiotica

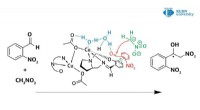
- Water speelt een cruciale rol in het mechanisme van de Henry-reactie gekatalyseerd door nieuwe kopercomplexen
 Waarom is de hoeveelheid zonnestraling die punten oppervlak ongelijk wordt verdeeld?
Waarom is de hoeveelheid zonnestraling die punten oppervlak ongelijk wordt verdeeld?  Wat zijn voorbeelden van een toename van entropie?
Wat zijn voorbeelden van een toename van entropie?  Wat gebeurt er als oceanische platen zich terugtrekken van het vasteland?
Wat gebeurt er als oceanische platen zich terugtrekken van het vasteland?  Welke term wordt aan elk chromosoom gegeven in een dubbel of gerepliceerd paar?
Welke term wordt aan elk chromosoom gegeven in een dubbel of gerepliceerd paar?  Gluren in een wereld van spin-3/2 materialen
Gluren in een wereld van spin-3/2 materialen Wat is de chemische formule voor calciumethanoaat?
Wat is de chemische formule voor calciumethanoaat?  Wat gebeurt er als je een chemische binding laat exploderen?
Wat gebeurt er als je een chemische binding laat exploderen? De delen van DNA die de code voor eiwitten bieden, zijn de?
De delen van DNA die de code voor eiwitten bieden, zijn de?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

