
Wetenschap
Gasvolume begrijpen:waarom het niet is opgelost
Hier is een overzicht van waarom:
* Gassen zijn samendrukbaar: In tegenstelling tot vaste stoffen en vloeistoffen liggen de moleculen in een gas ver uit elkaar. Dit betekent dat de afstand tussen gasmoleculen eenvoudig kan worden verkleind door druk uit te oefenen. Daarom kan het volume van een gas worden gewijzigd door de druk te veranderen.
* Gassen zetten uit om hun container te vullen: Gasmoleculen bewegen willekeurig en zijn niet op een bepaalde positie gefixeerd. Ze zullen zich verspreiden om het volledige volume van hun container te vullen. Dit is de reden waarom gassen geen vast volume hebben.
Dus hoewel gas geen vast volume heeft zoals een vaste stof of vloeistof, heeft het wel een specifiek volume bij een bepaalde temperatuur en druk. Dit wordt beschreven door de Ideale Gaswet, waarin staat:
PV =nRT
Waar:
* P is druk
* V is volume
* n is het aantal mol gas
* R is de ideale gasconstante
* T is temperatuur
Deze wet laat zien dat het volume van een gas recht evenredig is met de temperatuur en omgekeerd evenredig met de druk. Daarom kan het volume van een gas worden berekend als u de temperatuur, druk en hoeveelheid gas kent.
Samenvattend hebben gassen geen vast volume omdat ze samendrukbaar zijn en uitzetten om hun containers te vullen. Ze hebben echter wel een specifiek volume dat afhankelijk is van de temperatuur en druk.
 Een monster van 2.9990 g van een nieuwe verbinding is geanalyseerd en bevond zich de volgende massa's elementen koolstof 1.1610 waterstof 0.29240 zuurstof 1.5455 Bereken empirische formule?
Een monster van 2.9990 g van een nieuwe verbinding is geanalyseerd en bevond zich de volgende massa's elementen koolstof 1.1610 waterstof 0.29240 zuurstof 1.5455 Bereken empirische formule?  Wat betekent NaH3O2?
Wat betekent NaH3O2?  Wanneer alcohol en kwik koken, veranderen ze allebei van een vloeistof naar een?
Wanneer alcohol en kwik koken, veranderen ze allebei van een vloeistof naar een?  De omzetting van een vloeistof naar damp wanneer de druk gelijk is aan atmosferische druk?
De omzetting van een vloeistof naar damp wanneer de druk gelijk is aan atmosferische druk?  Wanneer gas in water verandert, wat gebeurt er?
Wanneer gas in water verandert, wat gebeurt er?
Hoofdlijnen
- Plantenveredeling:onzichtbare chromosomen gebruiken om pakketjes positieve eigenschappen door te geven
- Wat doen de cilia en flagellen in een cel?
- Nieuwe gegevens tonen de verspreiding van parasitaire hertenvliegen door de VS aan.
- Een membraan bestaat uit twee lagen lipidemoleculen. Wat de belangrijkste functie een celmembraan?
- Sleutelorganen van het uitscheidingssysteem:een uitgebreid overzicht
- Hoe wordt de productie van ATP in fotosynthese genoemd?
- Wat is de functie van een transportsysteem in het levende organisme?
- Wat is een weefsel dat luchtpassages lijnen?
- Onder welke toestand produceren spiercellen?
- Tarwegluten kunnen worden gebruikt om duurzaam luiermateriaal te maken

- Gefunctionaliseerde oppervlakken:cilindrische micellaire borstels met op maat gemaakte chemische opties met gecontroleerde lengte

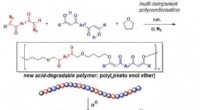
- Nieuw synthetisch polymeer afbreekbaar onder zeer milde zure omstandigheden
- De weg vrijmaken voor kunstmatige fotosynthese:effect van doping op de fotokatalysator SrTiO3

- Whisky verifiëren met laserlicht

 Wat wordt gebruikt om de stroom en het potentieelverschil in een circuit te regelen?
Wat wordt gebruikt om de stroom en het potentieelverschil in een circuit te regelen?  Hoeveel kwantumnummers?
Hoeveel kwantumnummers?  Welk instrument kan de hemelse lichamen duidelijk bekijken en zonder het effect van de atmosfeer van de aarde te filteren?
Welk instrument kan de hemelse lichamen duidelijk bekijken en zonder het effect van de atmosfeer van de aarde te filteren?  Sensoren op plantenbladeren waarschuwen voor watertekort
Sensoren op plantenbladeren waarschuwen voor watertekort Onderzoek toont aan dat online stemmen transformerend kan zijn voor inheemse gemeenschappen
Onderzoek toont aan dat online stemmen transformerend kan zijn voor inheemse gemeenschappen Wat is de atoommassa van Agbr?
Wat is de atoommassa van Agbr?  Wat is de energie van een 616 nm foton uitgezonden uit de lichtbron?
Wat is de energie van een 616 nm foton uitgezonden uit de lichtbron?  Hoe ziet de celdeling eruit?
Hoe ziet de celdeling eruit?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

