
Wetenschap
Kationische versus anionische ionen:groottefactoren uitgelegd
1. Nucleaire lading: Een hogere nucleaire lading (meer protonen in de kern) zal leiden tot een sterkere aantrekkingskracht op de elektronen, waardoor ze dichterbij worden getrokken en het ion kleiner wordt.
2. Aantal elektronen: Het verliezen van elektronen (het vormen van een kation) leidt over het algemeen tot een kleiner ion omdat er minder elektron-elektron-afstoting is. Het verkrijgen van elektronen (het vormen van een anion) leidt over het algemeen tot een groter ion vanwege de toegenomen elektron-elektron-afstoting.
3. Elektronenconfiguratie: De rangschikking van elektronen in de orbitalen beïnvloedt de grootte. Elektronen in de buitenste schillen ervaren minder aantrekkingskracht van de kern en dragen bij aan een groter ion.
Voorbeeld:
* Natrium (Na) versus natriumion (Na+): Natriumion is kleiner dan het neutrale natriumatoom omdat het een elektron heeft verloren, waardoor de elektron-elektron-afstoting wordt verminderd.
* Zuurstof (O) versus oxide-ion (O2-): Het oxide-ion is groter dan het neutrale zuurstofatoom omdat het twee elektronen heeft gewonnen, waardoor de elektron-elektron-afstoting toeneemt.
Daarom is het niet mogelijk om een algemene uitspraak te doen over het feit dat kationische moleculaire ionen altijd groter zijn dan anionische. De grootte van een ion hangt af van het specifieke element en het aantal gewonnen of verloren elektronen.
Belangrijke opmerking: Het concept van 'groter' kan ook verwijzen naar de kosten van het ion. In dat geval is het zo dat een kation een positieve lading heeft, terwijl een anion een negatieve lading heeft. Dit heeft echter geen betrekking op de grootte van de ionen.
 Feiten over de Atlantische kustvlaktes
Feiten over de Atlantische kustvlaktes Wat vertegenwoordigt de aarde?
Wat vertegenwoordigt de aarde?  Nieuwe kaart van Nederland laat zien waar stikstofreductie het meest effectief is
Nieuwe kaart van Nederland laat zien waar stikstofreductie het meest effectief is Hoe blootstelling aan negatieve feedback doelgericht consumentengedrag beïnvloedt
Hoe blootstelling aan negatieve feedback doelgericht consumentengedrag beïnvloedt  Amerikaanse hoorzitting over klimaatwetenschap vervalt in pestende voedselstrijd
Amerikaanse hoorzitting over klimaatwetenschap vervalt in pestende voedselstrijd
Hoofdlijnen
- Mitose bij mensen resulteert de vorming van wat?
- Wat is een soort en hoe ontwikkelen ze zich?
- Waar is de meniscus uit samengesteld?
- Aseksuele versus seksuele voortplanting:typen, verschillen en voorbeelden
- Kunnen uitwerpselen de soort redden?
- Wetenschappers zetten primaten tegenover zoogdieren met kleinere hersenen om erachter te komen wie de slimste verzamelaar is
- Woordproblemen schrijven voor Math
- Wat is de naam van organel die eiwitten en andere stoffen door cel verplaatst?
- Spindelvezels:de cytoskeletstructuren die verantwoordelijk zijn voor de scheiding van chromosomen
- Overgangsmetalen versus innerlijke overgangsmetalen:de belangrijkste verschillen verklaard
- Moleculaire sonde brengt verkeerd gevouwen proteoomstatus in levende cellen in kaart
- Wetenschappers hebben eiwitten gemaakt die worden gecontroleerd door licht
- Ingenieurs ontwikkelen recept om kogelvrije vesten drastisch te versterken

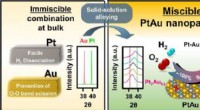
- Directe synthese van waterstofperoxide met een platina-gouden nanodeeltjeskatalysator
 Israël sluit Middellandse Zeekust nadat olie kust verwoest
Israël sluit Middellandse Zeekust nadat olie kust verwoest Wat heeft angst ermee te maken?
Wat heeft angst ermee te maken?  Iets dat beweert wetenschap te zijn, maar geen A wordt genoemd?
Iets dat beweert wetenschap te zijn, maar geen A wordt genoemd?  Wat is een voorbeeld van een geohazard?
Wat is een voorbeeld van een geohazard?  Synthese van zilveren nanodeeltjes met behulp van aardbeiboomblad
Synthese van zilveren nanodeeltjes met behulp van aardbeiboomblad Wat is het verschil tussen bioleaching en fytomining?
Wat is het verschil tussen bioleaching en fytomining?  Wat is de samenstelling van Milky Way Galaxy?
Wat is de samenstelling van Milky Way Galaxy?  Wat is het secundaire metabolisme in de plant?
Wat is het secundaire metabolisme in de plant?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

