
Wetenschap
Principes van elektronenconfiguratie:de regel van Aufbau en Hund uitgelegd
1. Aufbau-principe:
* Dit principe stelt dat elektronen orbitalen vullen in volgorde van toenemende energie. Dit betekent dat we beginnen met de orbitalen met de laagste energie en omhoog gaan.
* Energieniveaus worden bepaald door het hoofdkwantumgetal (n) en subniveaus worden bepaald door het azimutale kwantumgetal (l).
* De volgorde is:1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p.
2. Hunds regel:
* Deze regel stelt dat binnen een subshell (zoals de 2p-subshell) elektronen afzonderlijk elke orbitaal binnen die subshell zullen bezetten voordat ze zich in een bepaalde orbitaal verdubbelen.
* Dit komt omdat elektronen elkaar afstoten, en ze zijn het meest stabiel als ze zo ver mogelijk uit elkaar staan.
* Elektronen in verschillende orbitalen binnen dezelfde subshell hebben parallelle spins (allemaal spin omhoog of allemaal spin omlaag).
3. Pauli-uitsluitingsprincipe:
* Dit principe stelt dat geen twee elektronen in een atoom dezelfde set van vier kwantumgetallen kunnen hebben.
* Dit betekent dat elke orbitaal maximaal twee elektronen kan bevatten, en deze twee elektronen moeten tegengestelde spins hebben.
4. De "n + l"-regel (voor het bestellen van orbitalen):
* Deze regel is een handige manier om de volgorde van het vullen van orbitalen te onthouden, vooral voor grotere atomen.
* De regel stelt dat de orbitaal met de laagste waarde van (n + l) als eerste wordt gevuld. Als twee orbitalen dezelfde (n + l) waarde hebben, wordt de orbitaal met de lagere waarde van n als eerste gevuld.
Visueel hulpmiddel:de diagonale regel
* Je kunt de vulvolgorde van orbitalen visualiseren met de diagonaalregel . Dit is een handig diagram dat je helpt de volgorde van de orbitalen te onthouden op basis van hun energieniveaus.
Voorbeeld:
Laten we het element Stikstof (N) nemen, dat 7 elektronen heeft.
1. Aufbau-principe: Begin met het laagste energieniveau, 1s. Vul het met 2 elektronen (1s²).
2. Aufbau-principe: Ga naar het volgende laagste energieniveau, 2s. Vul het met 2 elektronen (2s²).
3. Aufbau-principe en de regel van Hund: Ga naar de 2p-subshell. Deze heeft 3 orbitalen (2px, 2py, 2pz). Plaats één elektron in elk van deze orbitalen, met parallelle spins, voordat je verdubbelt (2p³, 2p³, 2p³).
Daarom is de elektronenconfiguratie van stikstof 1s² 2s² 2p³.
Belangrijkste punten:
* Als u deze principes begrijpt, kunt u de elektronenconfiguratie van elk atoom voorspellen.
* Elektronenconfiguratie is cruciaal voor het begrijpen van het chemische gedrag en de eigenschappen van elementen.
* Het helpt ons de binding, reactiviteit en de periodieke trends van elementen te verklaren.
 Wat is de verhouding tussen suikerkoolstofatomen tot zuurstof?
Wat is de verhouding tussen suikerkoolstofatomen tot zuurstof?  H2O CO2 C12HO Zijn voorbeelden van wat?
H2O CO2 C12HO Zijn voorbeelden van wat?  Onderzoek biedt hoop op eenvoudigere diagnose en behandeling van kanker
Onderzoek biedt hoop op eenvoudigere diagnose en behandeling van kanker Is een fles veerwaterelementen samengesteld homogeen of heterogeen mengsel?
Is een fles veerwaterelementen samengesteld homogeen of heterogeen mengsel?  Waarom smolt je ijsblokje sneller in water dan zoete thee -spritmelk appelsap en cola op 70 graden?
Waarom smolt je ijsblokje sneller in water dan zoete thee -spritmelk appelsap en cola op 70 graden?
 Waterkoeling voor de aardkorst - zeewater dringt veel dieper door dan eerder werd gedacht
Waterkoeling voor de aardkorst - zeewater dringt veel dieper door dan eerder werd gedacht Plaats dit in bestelling Ecosysteem en gemeenschap van het populatieorganisme?
Plaats dit in bestelling Ecosysteem en gemeenschap van het populatieorganisme?  De erfenis van oude ijstijden bepaalt hoe zeegrassen vandaag de dag reageren op bedreigingen voor het milieu
De erfenis van oude ijstijden bepaalt hoe zeegrassen vandaag de dag reageren op bedreigingen voor het milieu  VS heeft de natste 12 maanden ooit - opnieuw
VS heeft de natste 12 maanden ooit - opnieuw AI onthult geheime wegen die de regenwouden van de wereld in gevaar brengen
AI onthult geheime wegen die de regenwouden van de wereld in gevaar brengen
Hoofdlijnen
- Welk deel regelt de activiteit van een cel?
- Is het proces exocytosis materialen die in een cel worden genomen?
- Wat zijn de methoden om een cel te bestuderen?
- Wat gebeurt er wanneer ziekteverwekkers van het ene oppervlak naar het andere worden overgebracht?
- Hoe vinden verteerde voedselmoleculen hun weg naar de cellen van het lichaam?
- Wat was de bruine klodder die zich vormde in het Stanley-laboratoriumexperiment?
- De rol van nucleïnezuren in een cel samenvatten?
- Ondanks de wet stijgt het aantal doden door loodvergiftiging in New Hampshire
- Wat zijn de primitieve soorten kunstmatige neuron?
- Video:Hoe chemie verwijdering van koolstofdioxide mogelijk maakt

- Onderzoekers hebben geheimen ontgrendeld over gemanipuleerde eiwitreceptoren, AUTO

- Vloeistof-vloeistof fasescheiding blijkt het proces van het omzetten van spidroïne-eiwitten in spinnenwebvezels te stimuleren
- Wetenschappers vinden potentiële ziektebestrijdende kernkoppen verborgen in bacteriën
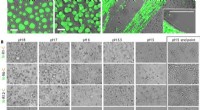
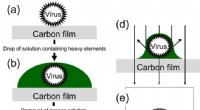
- Nieuw niet-radioactief, neutraal reagens onthult virussen in duidelijke details
 Wat is de staat dat energie nooit kan worden gemaakt of vernietigd?
Wat is de staat dat energie nooit kan worden gemaakt of vernietigd?  Verschijnt Thunder op andere planeten?
Verschijnt Thunder op andere planeten?  Wat is de chemische formule voor dihydrogen fluoride?
Wat is de chemische formule voor dihydrogen fluoride?  Wanneer de afstand van een geladen deeltje de sterkte van het elektrische veld waar of onwaar afneemt?
Wanneer de afstand van een geladen deeltje de sterkte van het elektrische veld waar of onwaar afneemt?  Zijn er cis-trans-isomeren gevormd wanneer waterige broom reageert met cyclohexeen?
Zijn er cis-trans-isomeren gevormd wanneer waterige broom reageert met cyclohexeen?  Wat wordt energie overgedragen via hete koude objecten?
Wat wordt energie overgedragen via hete koude objecten?  Wat voor soort energie komt van de radio?
Wat voor soort energie komt van de radio?  Op weg naar nieuwe veelbelovende ferro-elektrische materialen van het perovskiettype:hogedruksynthese van rubidiumniobaat
Op weg naar nieuwe veelbelovende ferro-elektrische materialen van het perovskiettype:hogedruksynthese van rubidiumniobaat
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

