
Wetenschap
Waterstofoxidatiegetallen:+1 en -1 begrijpen
* +1 Oxidatietoestand: Waterstof heeft doorgaans een oxidatiegetal van +1 wanneer het gebonden is aan niet-metalen. Dit komt omdat het de neiging heeft zijn enkele elektron te verliezen om een stabiele edelgasconfiguratie te bereiken. Voorbeelden:
* HCl: Waterstof is +1, chloor is -1.
* H₂O: Waterstof is +1, zuurstof is -2.
* -1 oxidatietoestand: Waterstof kan ook een oxidatiegetal van -1 hebben wanneer het aan metalen is gebonden. In deze gevallen krijgt waterstof een elektron om een stabiele configuratie te bereiken. Voorbeelden:
* NaH: Natrium is +1, waterstof is -1.
* LiH: Lithium is +1, waterstof is -1.
Belangrijkste punten om te onthouden:
* Elektronegativiteit: De oxidatietoestand van waterstof wordt bepaald door de relatieve elektronegativiteit van het element waaraan het is gebonden. Niet-metalen zijn elektronegatiever dan waterstof, dus waterstof wordt +1. Metalen zijn minder elektronegatief dan waterstof, dus waterstof wordt -1.
* Uitzonderingen: Er zijn enkele uitzonderingen op deze algemene regels, vooral in gevallen waarbij sprake is van covalente bindingen met elementen die qua elektronegativiteit vergelijkbaar zijn met waterstof.
 Ecosysteem van vijvers voor kinderen
Ecosysteem van vijvers voor kinderen  Waarom niet-geëxplodeerde munitie fysieke en ecologische risico's met zich meebrengt
Waarom niet-geëxplodeerde munitie fysieke en ecologische risico's met zich meebrengt  Puerto Rico mobiliseert terwijl potentiële orkaan nadert
Puerto Rico mobiliseert terwijl potentiële orkaan nadert Enorme piek in wereldwijde koolstofemissies gekoppeld aan El Nino
Enorme piek in wereldwijde koolstofemissies gekoppeld aan El Nino Branden verkolen range opzetten ranchers voor ontberingen in het westen van de VS
Branden verkolen range opzetten ranchers voor ontberingen in het westen van de VS
Hoofdlijnen
- Waarom heb je bouillon nodig om de bacteriën te verspreiden?
- Welk deel van de mannelijke reproductieve cel bevat erfelijke informatie die zal worden doorgegeven aan de baby?
- Hoe is een wetenschapper die licht bestudeert geroepen?
- Wat regelt het meest direct de snelheid waarmee voedsel wordt afgebroken om energie A enzymen B -hormonen C -nucleïnezuren D -vitamines vrij te geven?
- Hoe muizen de beste vluchtroute kiezen
- Wat is de commerciële toepassing van biologische producten?
- Waarom wordt natuurlijke selectie ook differentiaal of overleving genoemd?
- Handels in huisdieren en medicijnen die van invloed zijn op de plaatselijke tokay-gekkopopulaties, melden ecologen
- Wat is een waarneembaar kenmerk van Ester?
- Wetenschappers vinden mogelijke ontbrekende schakel in chemie die leidde tot leven op aarde

- Hoge sterkte gepultrudeerde thermoplastische composieten gemaakt van nieuwe grondstof

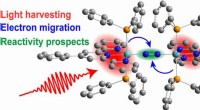
- Hoe zonlicht elektronen activeert om stikstof te breken en ammoniak te vormen
- Goedkoop, afdrukbaar 3D-apparaat ontworpen voor het analyseren van chemicaliën van smartphones

- Aan de lijn:kijken hoe nanodeeltjes vorm krijgen

 Kunstmatige bodems kunnen de sleutel zijn bij het herstel van de kolenmijnen in Latrobe Valley
Kunstmatige bodems kunnen de sleutel zijn bij het herstel van de kolenmijnen in Latrobe Valley Waarom zijn sterren geel?
Waarom zijn sterren geel?  Wat voor soort metamorfe rots is te vinden in de centrale Adirondacks?
Wat voor soort metamorfe rots is te vinden in de centrale Adirondacks?  Liggen de continenten en oceaanbekkens in de asthenosfeer?
Liggen de continenten en oceaanbekkens in de asthenosfeer?  Wat voor soort mengsel is deeg die ik nodig heb, hulpvraag?
Wat voor soort mengsel is deeg die ik nodig heb, hulpvraag?  Massaproductie van nieuwe klasse halfgeleiders dichter bij de realiteit
Massaproductie van nieuwe klasse halfgeleiders dichter bij de realiteit Lekke atmosfeer gekoppeld aan lichtgewicht planeet
Lekke atmosfeer gekoppeld aan lichtgewicht planeet Waarom hebben grotere organismen niet meer chromosomen nodig?
Waarom hebben grotere organismen niet meer chromosomen nodig?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

