
Wetenschap
Kooldioxide begrijpen:kookpunt versus sublimatie
* CO2 is een gas bij standaardtemperatuur en -druk. Het bestaat alleen als vloeistof of vaste stof onder zeer hoge druk.
* Sublimatie: In plaats van te koken gaat CO2 direct over van een vaste stof (droogijs) naar een gas bij een specifieke druk en temperatuur, het zogenaamde *sublimatiepunt*.
Dit is het overzicht:
* Sublimatiepunt: -78,5 °C (-109,3 °F) bij standaard atmosferische druk (1 atm). Bij deze temperatuur zal vast CO2 direct overgaan in gasvormig CO2, zonder een vloeibare fase te doorlopen.
* Kritisch punt: 31,1 °C (88 °F) en 73,8 bar (1071 psi). Boven dit punt kan CO2 niet vloeibaar worden gemaakt, ongeacht hoeveel druk er wordt uitgeoefend.
Dus in plaats van te praten over 'kooldioxide koken', verwijzen we naar het sublimatiepunt.
 Het instorten van het West-Antarctische ijs kan worden voorkomen door oceaanwater erop te laten sneeuwen
Het instorten van het West-Antarctische ijs kan worden voorkomen door oceaanwater erop te laten sneeuwen 'Ondernemersgeest':een product van nature of nurture?
'Ondernemersgeest':een product van nature of nurture?  Gegevens uit Kilauea suggereren dat de uitbarsting ongekend was
Gegevens uit Kilauea suggereren dat de uitbarsting ongekend was Waar kan het klimaat worden bestuurd door?
Waar kan het klimaat worden bestuurd door?  Broeikasgasanalyses maken op de weg, eh, rails
Broeikasgasanalyses maken op de weg, eh, rails
Hoofdlijnen
- Welke chromosomen draagt het minste aantal genen?
- Waarom denken wetenschappers dat de omstandigheden voor het leven kunnen bestaan binnen Enceladus?
- Naam van de vloeistof in het menselijk oor?
- Hoe kan een polaire geneeskunde zich anders in uw lichaam gedragen dan niet -polair?
- Waarvoor gebruikt het lichaam nucleïnezuren?
- Hoe ondersteunen celstructuren functie?
- Waarom het een goed idee is om met je dronken oom over politiek te praten
- Wat hondeneigenaren moeten weten over leptospirose
- Wanneer heeft Schwann veel verschillende dierencellen waargenomen en tot een conclusie gekomen?
- Labelen en detecteren van RNA-modificaties

- Moleculaire structuur van anti-verouderingseiwit alfa Klothos onthuld

- Het beheersen van de nanoschaalstructuur van membranen is essentieel voor schoon water, onderzoekers vinden

- Een verborgen elektronische overgang van S0 naar Tn in moleculen die zware atomen bevatten

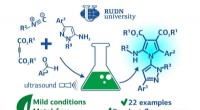
- Chemicus stelt milieuvriendelijke synthese van fluorescerende verbindingen voor medicijnen voor
 Wat gebeurt er met de snelheden van een golf als deze weerspiegelt?
Wat gebeurt er met de snelheden van een golf als deze weerspiegelt?  We zitten in een El Niño. Waarom is Australië zo nat geweest?
We zitten in een El Niño. Waarom is Australië zo nat geweest?  Welke menselijke activiteiten hebben een negatief effect op de oceaan?
Welke menselijke activiteiten hebben een negatief effect op de oceaan?  Wat is de krachtigste methode van erosie?
Wat is de krachtigste methode van erosie?  Bioluminescentie ontstond minstens 540 miljoen jaar geleden voor het eerst bij dieren, waardoor het oudste, gedateerde voorbeeld werd teruggedrongen
Bioluminescentie ontstond minstens 540 miljoen jaar geleden voor het eerst bij dieren, waardoor het oudste, gedateerde voorbeeld werd teruggedrongen  Effectief personeelsbeheer van essentieel belang voor luchtsteun van de politie, blijkt uit onderzoek
Effectief personeelsbeheer van essentieel belang voor luchtsteun van de politie, blijkt uit onderzoek Wat zijn 4 dingen die u in zand zou kunnen waarnemen, worden opgesteld uit calciet?
Wat zijn 4 dingen die u in zand zou kunnen waarnemen, worden opgesteld uit calciet?  Protisten hebben wat intermediaire mitotische organisatie wordt genoemd. Wat is de meest waarschijnlijke hypothese over deze vormen van celdeling?
Protisten hebben wat intermediaire mitotische organisatie wordt genoemd. Wat is de meest waarschijnlijke hypothese over deze vormen van celdeling?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

