
Wetenschap
Berekening van de normaliteit van H₂SO₄:een stapsgewijze handleiding
Zo bereken je de normaliteit van een 1,25 M oplossing van H₂SO₄:
Normaliteit begrijpen
* Normaliteit (N) is een concentratiemaat die het aantal equivalenten van een opgeloste stof per liter oplossing uitdrukt.
* Equivalenten zijn mol van een stof die kan reageren met één mol waterstofionen (H⁺) of deze kan vervangen in een zuur-base-reactie.
De normaliteit van H₂SO₄ berekenen
1. Identificeer het aantal zure waterstofionen (H⁺) per molecuul: H₂SO₄ heeft twee zure waterstofionen.
2. Vermenigvuldig de molariteit met het aantal zure waterstofionen:
Normaliteit (N) =Molariteit (M) * Aantal H⁺-ionen
N =1,25 M * 2 =2,5 N
Daarom is de normaliteit van een 1,25 M oplossing van H₂SO₄ 2,5 N.
 Zijn vaatwasserpods veilig? De wetenschap achter PVA en de impact op het milieu
Zijn vaatwasserpods veilig? De wetenschap achter PVA en de impact op het milieu  Gemanipuleerde microben kunnen biologisch afbreekbare kunststoffen produceren tegen lagere kosten en milieu-impact dan plantaardige kunststoffen
Gemanipuleerde microben kunnen biologisch afbreekbare kunststoffen produceren tegen lagere kosten en milieu-impact dan plantaardige kunststoffen Hoe bouwen bacteriën natuurlijke producten op?
Hoe bouwen bacteriën natuurlijke producten op? Hoe is enthalpie gerelateerd aan het spontaan van een reactie?
Hoe is enthalpie gerelateerd aan het spontaan van een reactie?  HCl-concentratie en antacidum-titratie:impact op molberekeningen
HCl-concentratie en antacidum-titratie:impact op molberekeningen
 Terwijl Phoenix sist, stedelijk eilandfenomeen vermengt warmte (update)
Terwijl Phoenix sist, stedelijk eilandfenomeen vermengt warmte (update) Welk zeebioom wordt gekenmerkt door diepe waterdiepten die nooit zonlicht ontvangen?
Welk zeebioom wordt gekenmerkt door diepe waterdiepten die nooit zonlicht ontvangen?  Zeekaarten uit de 18e eeuw onthullen koraalverlies
Zeekaarten uit de 18e eeuw onthullen koraalverlies Hoe op de natuur gebaseerde kennis lokale ecosystemen kan herstellen en het welzijn van de gemeenschap kan verbeteren
Hoe op de natuur gebaseerde kennis lokale ecosystemen kan herstellen en het welzijn van de gemeenschap kan verbeteren  Megadrought veroorzaakte mega verlies aan biodiversiteit
Megadrought veroorzaakte mega verlies aan biodiversiteit
Hoofdlijnen
- Gebruikt een nucleotide eiwit?
- Hoe zou je een grote koloniale organismen onderscheiden van meercellig organisme?
- Wat is het verschil tussen planten, schimmels en dieren?
- Wat produceert bemesting van plantengameten?
- Slapen spinnen? Uit onderzoek blijkt dat ze net als mensen kunnen dutten
- Wat is de functie van vasculaire weefsels in planten?
- Hoe een verandering van één gen leidde tot nieuwe soorten Monkeyflower
- Waar verbouw je microben in?
- Worden DNA -genomen gevonden in alle organismen en virussen?
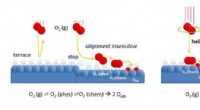
- We begrijpen eindelijk hoe zuurstof reageert op platina
- Het versnellen van kopercorrosie op een cent:een wetenschappelijke stapsgewijze handleiding

- Technologie verandert smartphones in on-the-spot detectoren voor door voedsel overgedragen ziekten, andere gevaarlijke verontreinigingen

- Een uitgebreide kijk op koemelk

- Serendipiteitsexperiment in de achtertuin werpt licht op de productie van polymeren
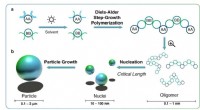
 Was de oersoep een stevige pre-eiwitstoofpot?
Was de oersoep een stevige pre-eiwitstoofpot?  Wat zijn de 2 microscopische organismen die ziekten veroorzaken?
Wat zijn de 2 microscopische organismen die ziekten veroorzaken?  Wat zijn 5 voorbeelden van oplosmiddelen?
Wat zijn 5 voorbeelden van oplosmiddelen?  Nieuwe methode maakt gebruik van nanofibrillen op magnetische microdeeltjes om HIV-deeltjes te isoleren
Nieuwe methode maakt gebruik van nanofibrillen op magnetische microdeeltjes om HIV-deeltjes te isoleren  Hoe scheiden Vissen vissen af?
Hoe scheiden Vissen vissen af?  Wat zijn vijf voorbeelden van kinetische energie?
Wat zijn vijf voorbeelden van kinetische energie?  Hoe Steam Flow naar Megawatt te converteren
Hoe Steam Flow naar Megawatt te converteren  Wanneer statische elektriciteit snel wordt geloosd, welke vormen van energie kunnen worden geproduceerd?
Wanneer statische elektriciteit snel wordt geloosd, welke vormen van energie kunnen worden geproduceerd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

