
Wetenschap
Propanolverbrandingsvergelijkingen:compleet en onvolledig - Chemie uitgelegd
Volledige verbranding
* Reactanten: Propanol (C₃H₇OH) en zuurstof (O₂)
* Producten: Kooldioxide (CO₂), water (H₂O) en energie (warmte)
Gebalanceerde vergelijking:
2 C₃H₇OH + 9 O₂ → 6 CO₂ + 8 H₂O + Energie
Uitleg:
* De coëfficiënten vóór elk molecuul zorgen ervoor dat het aantal atomen van elk element aan beide kanten van de vergelijking gelijk is.
* Volledige verbranding vindt plaats wanneer er voldoende zuurstof is om met alle brandstof te reageren. Alle koolstofatomen in propanol worden geoxideerd om CO₂ te vormen.
Onvolledige verbranding
* Reactanten: Propanol (C₃H₇OH) en zuurstof (O₂)
* Producten: Koolmonoxide (CO), kooldioxide (CO₂), water (H₂O) en energie (warmte)
Gebalanceerde vergelijking (één mogelijke optie):
2 C₃H₇OH + 7 O₂ → 4 CO₂ + 2 CO + 8 H₂O + Energie
Uitleg:
* Onvolledige verbranding vindt plaats wanneer er niet genoeg zuurstof is om de brandstof volledig te oxideren.
*Dit leidt tot de vorming van koolmonoxide (CO), een giftig gas, naast kooldioxide.
*De exacte verhouding tussen geproduceerd CO₂ en CO kan variëren, afhankelijk van de beschikbaarheid van zuurstof.
Belangrijke opmerking: Onvolledige verbranding is minder efficiënt in termen van vrijkomende energie en produceert schadelijke bijproducten. Het is over het algemeen ongewenst, vooral in afgesloten ruimtes.
 Nieuwe analyse benadrukt belang van grondwaterafvoer in oceanen
Nieuwe analyse benadrukt belang van grondwaterafvoer in oceanen Hoe beïnvloedt zure regen de natuur?
Hoe beïnvloedt zure regen de natuur?  Portugal worstelt om uit de as van zijn dodelijkste vuur te herrijzen
Portugal worstelt om uit de as van zijn dodelijkste vuur te herrijzen Voedingsstof op de diepzeebodem van vitaal belang in de wereldwijde voedselketen
Voedingsstof op de diepzeebodem van vitaal belang in de wereldwijde voedselketen Nepal lijkt toegang tot Everest te beperken na sterfgevallen, maar twijfels blijven hangen
Nepal lijkt toegang tot Everest te beperken na sterfgevallen, maar twijfels blijven hangen
Hoofdlijnen
- Wordt celdeling gevonden in de kernchromosomen?
- Hoe gastheercelenzymen het coronavirus bestrijden
- Welke DNA -code kan een kopie van zichzelf maken?
- Hoe lossen we het probleem van de afvoer van nutriënten in de landbouw op?
- Hoe verschillen meiose en mitose?
- Waarom we vleermuizen niet zo snel moeten demoniseren
- Is het verschil tussen glycogeen en zetmeel?
- Wat zijn vier subcellulaire organellen?
- Wat voor soort schimmels zijn niet meercellig?
- Studie initieert chemische reacties door materialen te koelen in plaats van ze te verwarmen
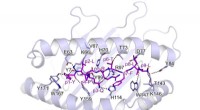
- Ontdekken hoe T-cellen het SARS-COV-2 virus spike-eiwit herkennen
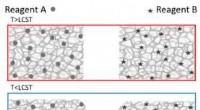
- Schadelijke moleculen detecteren met licht

- Beoordeling van technologieën die het potentieel voor de omzetting van kooldioxide in bruikbare producten vergroten
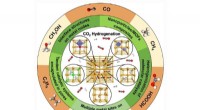
- Onderzoekers simuleren dynamische auto-emissies met behulp van gouden nanodeeltjes voor katalyse

 Als er intelligente buitenaardse wezens bestaan, waarom hebben we ze dan niet gezien?
Als er intelligente buitenaardse wezens bestaan, waarom hebben we ze dan niet gezien?  Wat zijn de vijf voorbeelden van fundamentele grootheden?
Wat zijn de vijf voorbeelden van fundamentele grootheden?  Studenten ontwerpen 3D-geprint optisch kaartsysteem
Studenten ontwerpen 3D-geprint optisch kaartsysteem Nanodraden gemaakt van gespannen silicium laten zien hoe de toename van het computervermogen kan blijven komen
Nanodraden gemaakt van gespannen silicium laten zien hoe de toename van het computervermogen kan blijven komen Welk type zonnestraling is het minst krachtig?
Welk type zonnestraling is het minst krachtig?  Wat is de letterlijke betekenis van maag in de biologie?
Wat is de letterlijke betekenis van maag in de biologie?  Twee muziekbloemlezingen nu voor eeuwig opgeslagen in DNA
Twee muziekbloemlezingen nu voor eeuwig opgeslagen in DNA Is alle pijn mentaal?
Is alle pijn mentaal?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

