
Wetenschap
Covalente verbindingen bij kamertemperatuur:fysische toestanden verklaard
* De sterkte van de covalente bindingen: Sterkere bindingen leiden tot hogere smelt- en kookpunten.
* De grootte en vorm van het molecuul: Grotere moleculen hebben een groter oppervlak voor intermoleculaire krachten, wat leidt tot hogere smelt- en kookpunten.
* De polariteit van het molecuul: Polaire moleculen hebben sterkere intermoleculaire krachten dan niet-polaire moleculen, wat leidt tot hogere smelt- en kookpunten.
Algemene trends:
* Gassen: Covalente verbindingen met zeer zwakke intermoleculaire krachten zijn doorgaans gassen bij kamertemperatuur. Voorbeelden hiervan zijn methaan (CH4), kooldioxide (CO2) en stikstof (N2).
* Vloeistoffen: Covalente verbindingen met matige intermoleculaire krachten zijn doorgaans vloeistoffen bij kamertemperatuur. Voorbeelden hiervan zijn water (H2O), ethanol (C2H5OH) en aceton (CH3COCH3).
* Vaste stoffen: Covalente verbindingen met sterke intermoleculaire krachten zijn doorgaans vaste stoffen bij kamertemperatuur. Voorbeelden hiervan zijn suiker (C12H22O11), diamant (C) en siliciumdioxide (SiO2).
Uitzonderingen:
* Netwerkvolumes: Sommige covalente verbindingen vormen gigantische structuren met sterke covalente bindingen door de hele structuur. Deze zijn doorgaans erg hard en hebben zeer hoge smeltpunten, zoals diamant en siliciumcarbide.
* Kleine, zeer polaire moleculen: Sommige kleine, zeer polaire covalente moleculen kunnen sterke intermoleculaire krachten hebben, wat leidt tot hogere smelt- en kookpunten. Voorbeelden hiervan zijn water (H2O) en waterstoffluoride (HF).
Samenvattend:
Hoewel er geen enkele "gebruikelijke toestand" bestaat voor covalente verbindingen bij kamertemperatuur, zal het merendeel ervan gassen, vloeistoffen of vaste stoffen zijn. afhankelijk van de hierboven genoemde factoren.
 In een gekatalyseerde reactie wordt raectanten vaak een genoemd?
In een gekatalyseerde reactie wordt raectanten vaak een genoemd?  Wat is een deeltje in een atoom met neutrale lading?
Wat is een deeltje in een atoom met neutrale lading?  Wat voor soort mengsel is ijzer?
Wat voor soort mengsel is ijzer?  Wat is de naam van de methode waarmee warmte door vloeistof en gas reist?
Wat is de naam van de methode waarmee warmte door vloeistof en gas reist?  Hoe verandert de beweging van watermoleculen wanneer vloeistof naar gas wordt gevormd?
Hoe verandert de beweging van watermoleculen wanneer vloeistof naar gas wordt gevormd?
Hoofdlijnen
- Wat eindigt de vertaling in DNA?
- Wat is de belangrijkste rol van eiwitten in het lichaam?
- Hoe zijn plantencellen zowel dier als bacterieel?
- Welk lichaamssysteem is verantwoordelijk voor het produceren van enzymen die helpen om stoffen af te breken om de groei en reparatie op te nemen?
- Anatomie en fysiologie van een synapsenstructuur
- Onderzoekers bieden visserij een oplossing voor overbevissing
- Meisjes zullen jongens zijn:geslachtsverandering bij drakenhagedissen
- Welke naam wordt gegeven aan het organisme dat zich van afzonderlijke cellen tot vele soorten cellen ontwikkelt?
- Beschrijf een reden waarom wetenschapper onderzoek zou kunnen doen?
- Smaakonderzoek voor consumentenbescherming

- Nieuwe inzichten in fermentatie-enzymen zullen de ecologische voetafdruk van de chemische industrie verkleinen
- Levensduur van brandstofcellen gemaximaliseerd met kleine hoeveelheden metalen
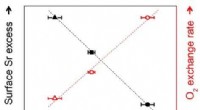
- Zelfmontage vereist:neutronen onderzoeken nieuw polymeergedrag voor biomedische materialen

- Wetenschappers onderzoeken de structuur van een sleutelgebied van telomerase-eiwit met een lange levensduur
 Kunnen symbiotische microben ecosystemen helpen de opwarming van de aarde te overleven?
Kunnen symbiotische microben ecosystemen helpen de opwarming van de aarde te overleven? Wat is de fysieke betekenis van planken constant?
Wat is de fysieke betekenis van planken constant?  Toplab CERN lanceert belangrijke nieuwe accelerator
Toplab CERN lanceert belangrijke nieuwe accelerator Waarom is landen op de maan anders dan op aarde?
Waarom is landen op de maan anders dan op aarde?  Wat is gencombinatie in de nakomelingen?
Wat is gencombinatie in de nakomelingen?  De hormonen worden door het bloed van bloedsomloop gedragen naar genetisch geconditioneerd?
De hormonen worden door het bloed van bloedsomloop gedragen naar genetisch geconditioneerd?  Wat is gravitatinale potetiale energie?
Wat is gravitatinale potetiale energie?  Afbeelding:Vega lofts Kalkoenen Aardobservatiesatelliet
Afbeelding:Vega lofts Kalkoenen Aardobservatiesatelliet
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

