
Wetenschap
Inzicht in de fysieke toestanden van covalente verbindingen
Covalente verbindingen worden gevormd door het delen van elektronen tussen atomen. De toestand van een covalente verbinding (vast, vloeibaar of gas) hangt van verschillende factoren af, waaronder:
* Kracht van intermoleculaire krachten: Deze krachten zijn de aantrekkingen tussen moleculen. Sterkere intermoleculaire krachten leiden tot een hoger smelt- en kookpunt, waardoor de kans groter is dat de verbinding vast is bij kamertemperatuur.
* Moleculaire grootte en vorm: Grotere moleculen en complexere vormen hebben over het algemeen sterkere intermoleculaire krachten.
* Polariteit: Polaire moleculen (met een ongelijkmatige verdeling van de elektronendichtheid) hebben sterkere dipool-dipoolkrachten, die bij kamertemperatuur tot een vloeibare of vaste toestand kunnen leiden.
Hier volgen enkele algemene trends:
* Gassen: Kleine, niet-polaire covalente moleculen zoals methaan (CH4) en koolstofdioxide (CO2) zijn gassen bij kamertemperatuur.
* Vloeistoffen: Veel covalente verbindingen met matige intermoleculaire krachten zijn vloeistoffen bij kamertemperatuur, zoals water (H2O) en ethanol (C2H5OH).
* Vaste stoffen: Covalente verbindingen met grote moleculen, sterke intermoleculaire krachten of netwerkstructuren (zoals diamanten of siliciumdioxide) zijn bij kamertemperatuur meestal vaste stoffen.
Het is belangrijk om te onthouden: Er zijn uitzonderingen op deze algemene trends, en de toestand van een bepaalde covalente verbinding kan variëren afhankelijk van de specifieke omstandigheden (temperatuur en druk).
Laat het me weten als je meer details wilt over een specifieke covalente verbinding!
 Welke eigenschap maakt bepaalde metalloïden nuttig als geschakeld om een kleine elektrische stroom uit te schakelen?
Welke eigenschap maakt bepaalde metalloïden nuttig als geschakeld om een kleine elektrische stroom uit te schakelen?  Batterijmaterialen in kaart brengen met atomaire precisie
Batterijmaterialen in kaart brengen met atomaire precisie Wat is de faseverschuiving van gas naar een vaste vorm?
Wat is de faseverschuiving van gas naar een vaste vorm?  Wat was de belangrijkste bijdrage aan de atoomtheorie?
Wat was de belangrijkste bijdrage aan de atoomtheorie?  Wat is substraatconcentratie?
Wat is substraatconcentratie?
 Waarom is het meest prachtige ding in de schepping?
Waarom is het meest prachtige ding in de schepping?  Wat is de zon voor een plant?
Wat is de zon voor een plant?  Wetenschappers over klimaatrisico's verbinden de droogte in Four Corners van 2018 rechtstreeks met door de mens veroorzaakte klimaatverandering
Wetenschappers over klimaatrisico's verbinden de droogte in Four Corners van 2018 rechtstreeks met door de mens veroorzaakte klimaatverandering Tools en technieken om methaan te volgen en te bestuderen
Tools en technieken om methaan te volgen en te bestuderen Gouverneur van Californië overweegt waterplan met één tunnel
Gouverneur van Californië overweegt waterplan met één tunnel
Hoofdlijnen
- Wat is de vernietiging van pathogeen mircorganisme, maar niet hun sporen?
- Hoe de uitvinding van de microscoop. Heeft wetenschappers geholpen cellen te begrijpen?
- Wie gebruikt de microscoop?
- Wat is het oudste celtype?
- Om de biosfeer voor toekomstige generaties te behouden, moeten mensen -?
- Wat is de groepsnaam in taxonomie voor een soort levende dingen die nakomelingen reproduceren kan reproduceren?
- Fotosynthese versus ademhaling:hoe het leven licht en zuurstof omzet in energie
- Waarom worden experimenten waarbij transplanterende soorten worden uitgevoerd die vandaag zelden worden uitgevoerd?
- Waarom is het belangrijk voor wetenschapper om hun resultaten te communiceren?
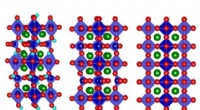
- Elektrische warmteklep:Strontiumkobaltoxide dunne film verandert thermische eigenschappen met aangelegde spanning
- Hoe u de calorimeterconstante kunt berekenen:een stapsgewijze handleiding

- Nieuwe methode biedt stabieler, efficiënte elektrokatalytische reacties
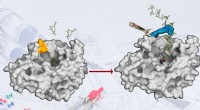
- Nieuwe technologie voor enzymontwerp
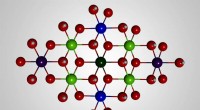
- Onderzoek onthult mechanisme achter watersplitsende katalysator
 Langere droge zomerperiode waargenomen in het regenwoud van Congo
Langere droge zomerperiode waargenomen in het regenwoud van Congo Is de zwaartekracht op een projectiel in beweging als positief beschouwd.?
Is de zwaartekracht op een projectiel in beweging als positief beschouwd.?  Waarom is ijs minder dicht dan vloeibare vorm?
Waarom is ijs minder dicht dan vloeibare vorm?  Waar is golfenergie geconcentreerd tijdens breking?
Waar is golfenergie geconcentreerd tijdens breking?  Hoe laadstroom te berekenen
Hoe laadstroom te berekenen  NaCl H2o- fysische of chemische verandering?
NaCl H2o- fysische of chemische verandering?  Boze politici maken boze kiezers, nieuwe studie vondsten
Boze politici maken boze kiezers, nieuwe studie vondsten Nieuwe gegevens laten zien hoe staten het doen in de wetenschap
Nieuwe gegevens laten zien hoe staten het doen in de wetenschap
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

