
Wetenschap
Berekening van beperkend reagens:MgCl₂ + 2KOH-reactie
1. Evenwichtige chemische vergelijking:
De uitgebalanceerde chemische vergelijking is:
MgCl₂ + 2KOH → Mg(OH)₂ + 2KCl
2. Molverhouding:
Uit de vergelijking blijkt dat 1 mol MgCl2 reageert met 2 mol KOH.
3. Bereken het aantal benodigde mol KOH:
Omdat je 6 mol MgCl₂ hebt, heb je 6 mol * 2 =12 mol KOH nodig om volledig te reageren.
4. Bepaal het beperkende reagens:
* Als u minder dan 12 mol KOH heeft: KOH is het beperkende reagens, omdat je niet genoeg hebt om met alle MgCl₂ te reageren.
* Als u 12 mol of meer KOH heeft: MgCl₂ is het beperkende reagens omdat je genoeg KOH hebt om met alle MgCl₂ te reageren.
Conclusie:
U moet de hoeveelheid KOH (in mol) opgeven om het beperkende reagens te bepalen.
 Voorlopers van een catastrofale ineenstorting
Voorlopers van een catastrofale ineenstorting Maatregelen om soorten te helpen omgaan met klimaatverandering?
Maatregelen om soorten te helpen omgaan met klimaatverandering?  De manier waarop mensen zich voor een kunstwerk bewegen, kan hun ervaring beïnvloeden
De manier waarop mensen zich voor een kunstwerk bewegen, kan hun ervaring beïnvloeden  Ha Long heli:Vietnam lanceert helikopterritten in beroemde baai
Ha Long heli:Vietnam lanceert helikopterritten in beroemde baai Britse pesticidennormen kunnen worden verlaagd in nieuwe handelsovereenkomsten, bedreiging voor de volksgezondheid en het milieu
Britse pesticidennormen kunnen worden verlaagd in nieuwe handelsovereenkomsten, bedreiging voor de volksgezondheid en het milieu
Hoofdlijnen
- De ontdekking van cellen is het meest direct gekoppeld van de ontwikkeling de?
- Hoeveel dochtercellen worden respectievelijk geproduceerd door mitose en meiose?
- Bindweefselcellen die fagocytisch zijn?
- Wat is de wetenschappelijke naam of taxonomische classificatie van jaarlijkse bloemenimpatiens?
- Waarom moet de cel zijn DNA voor mitose repliceren?
- Op welke manier controleert de samenleving de wetenschap?
- Wat deed Linnaeus om de evolutietheorie te helpen ontwikkelen?
- Wat zijn episamische organismen?
- Wat voor soort reproductieve treedt op wanneer dieren kloon nakomelingen produceren?
- Radioactieve massa omzetten in activiteit:een stapsgewijze handleiding van gram naar curie

- Basissen in de chemie begrijpen:definities, eigenschappen en toepassingen

- Chemici verkrijgen nieuw materiaal voor antibacteriële voedselcoatings
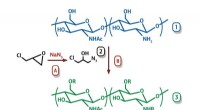
- Zilverzout dat wordt gebruikt om C-C-bindingen in ongespannen cyclische aminen te verbreken
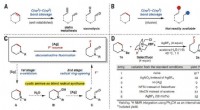
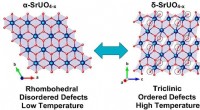
- Uranium gebruiken om orde te scheppen in wanorde
 Hoogwaardige en duurzame lithium-ionbatterij met verbeterde prestaties bij lage temperaturen door een prelithiatiestrategie
Hoogwaardige en duurzame lithium-ionbatterij met verbeterde prestaties bij lage temperaturen door een prelithiatiestrategie Lijst met ecosystemen
Lijst met ecosystemen  Hoe exoskeletten zullen werken
Hoe exoskeletten zullen werken  Hoe was de telescoop succesvol?
Hoe was de telescoop succesvol?  Is de zon -energiebron die in een voedselketen drijft?
Is de zon -energiebron die in een voedselketen drijft?  Axial Force
Axial Force Wat doen energiebronnen?
Wat doen energiebronnen?  Buitensporig risicovol krediet dat sterk verband houdt met de huisvestingscrisis van de afgelopen decennia, studie zegt:
Buitensporig risicovol krediet dat sterk verband houdt met de huisvestingscrisis van de afgelopen decennia, studie zegt:
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

