
Wetenschap
Radioactieve massa omzetten in activiteit:een stapsgewijze handleiding van gram naar curie
Door David Robinson • Bijgewerkt op 24 maart 2022
Radioactieve elementen vervallen met snelheden die traditioneel in curies werden gemeten. De International Council of Scientific Unions definieert één curie als de activiteit van een stof die 3,7 × 10¹⁰ desintegraties per seconde ondergaat. Omdat de vervalsnelheden per element variëren, is het omzetten van een massa in grammen naar curies alleen mogelijk als de exacte isotoop bekend is.
Stap 1
Zoek het atoomgewicht van de isotoop uit het periodiek systeem. Kobalt-60 heeft bijvoorbeeld een atoomgewicht van 59,92, terwijl uranium-238 een atoomgewicht van 238 heeft.
Stap 2
Converteer de massa naar mol:mol =massa / atoommassa. Vermenigvuldig vervolgens met het getal van Avogadro (6,02 × 10²³) om het aantal atomen te verkrijgen. 1 g Cobalt-60 levert bijvoorbeeld (1/59,92) × 6,02 × 10²³ ≈ 1,01 × 10²² atomen op.
Stap 3
Bereken de vervalsnelheid (r) met behulp van de activiteit van de isotoop. Voor Cobalt-60 met een activiteit van 1,10 × 10³ Ci, r = activiteit × (3,700 × 10¹⁰ atomen s⁻¹ Ci⁻¹) = 4,04 × 10¹³ atomen s⁻¹.
Stap 4
Bepaal de vervalconstante (k) uit de eerste-orde snelheidsvergelijking r =k x [aantal atomen]. Het gebruik van r = 4,04 × 10¹³ en 1,01 × 10²² atomen geeft k ≈ 4,1 × 10⁻⁹ s⁻¹.
Stap 5
Bereken de activiteit van het monster:activiteit =k x [aantal atomen]. Voor 1,01 × 10²² atomen, activiteit = 4,1 × 10⁻⁹ s⁻¹ × 1,01 × 10²² ≈ 4,141 × 10¹³ atomen s⁻¹.
Stap 6
Converteer de vervalsnelheid naar curies door te delen door 3,7 × 10¹⁰. Dus 1 g Cobalt-60 komt overeen met 4,141 × 10¹³ / 3,7 × 10¹⁰ ≈ 1.119 Ci.
TL;DR (te lang; niet gelezen)
Gebruik een wetenschappelijke rekenmachine en voer alle berekeningen in wetenschappelijke notatie uit om fouten bij het verwerken van grote getallen te voorkomen.
Waarschuwing
Stap 4 omvat calculus en vereist geavanceerde wiskundige kennis.
 Chemische reacties versus fysieke scheidingen:verbindingen begrijpen
Chemische reacties versus fysieke scheidingen:verbindingen begrijpen  Hoe Crucibles te reinigen
Hoe Crucibles te reinigen  Schudden, rammelaar, en rol naar hoogrenderende fotovoltaïsche energie
Schudden, rammelaar, en rol naar hoogrenderende fotovoltaïsche energie Onthulling van het effect van Ti-substituties op het statische oxidatiegedrag van (Hf,Ti)C bij 2500°C
Onthulling van het effect van Ti-substituties op het statische oxidatiegedrag van (Hf,Ti)C bij 2500°C  Hoeveel gram koper(II)sulfaat-pentahydraat zou je moeten meten om 10,0 watervrij koper(II)sulfaat te verkrijgen?
Hoeveel gram koper(II)sulfaat-pentahydraat zou je moeten meten om 10,0 watervrij koper(II)sulfaat te verkrijgen?
 Glacial engineering zou de zeespiegelstijging kunnen beperken, als we onze uitstoot onder controle krijgen
Glacial engineering zou de zeespiegelstijging kunnen beperken, als we onze uitstoot onder controle krijgen Hoe alpengraslanden reageren op klimaatverandering en antropogene effecten
Hoe alpengraslanden reageren op klimaatverandering en antropogene effecten Onderzoekers beschrijven een uniek systeem om te testen hoe goed smalle golfbanden van UV-licht ziektekiemen doden
Onderzoekers beschrijven een uniek systeem om te testen hoe goed smalle golfbanden van UV-licht ziektekiemen doden Klimaatcrisis veroorzaakt piek in doden door blikseminslag in India
Klimaatcrisis veroorzaakt piek in doden door blikseminslag in India Waarom hebben bomen in de rechte stammen en weinig lagere takken?
Waarom hebben bomen in de rechte stammen en weinig lagere takken?
Hoofdlijnen
- Wat is de wetenschap van het classificeren van levende wezens?
- Uw naam betekent gekleurde lichamen en u bevat DNA -doorgeven van eigenschappen aan nieuwe cellen op een systematische manier. Wat ben je?
- Een vogel in de bush is $223 waard, 851 in de hand
- Wat zijn specifieke biotechnologietoepassingen voor DNA-vingerafdrukken?
- Wat is het xylom en Phoelom?
- Nieuwe coronavirussen zijn het meest riskant voor overloop
- Genetische technologie onthult hoe giftige paddenstoelen gifstoffen produceren
- Verschil tussen koppelingstoewijzing en chromosoommapping
- Gene-interferentie berekenen:een praktische gids voor crossover-analyse
- De scheikundige laat zien dat intermoleculaire interacties voorheen onbekende dimensies kunnen bereiken

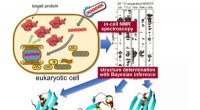
- In-situ meting van 3D-eiwitstructuur in levende eukaryote cellen
- Video:Hoe dubbelwerkend bakpoeder twee keer werkt

- Het toevoegen van een inert polymeer aan plastic zonnecellen zorgt voor een hoog rendement en eenvoudige productie

- Sneller en groener zuiveringsproces met kooldioxide

 Hoe drukt u 0,0247 goed uit in wetenschappelijke notatie?
Hoe drukt u 0,0247 goed uit in wetenschappelijke notatie?  Naam onderdelen van het reproductieve systeem van planten?
Naam onderdelen van het reproductieve systeem van planten?  Op welke van de volgende manieren beïnvloeden erosie en afzetting de oceanen?
Op welke van de volgende manieren beïnvloeden erosie en afzetting de oceanen?  Grootste politiemacht in de VS stapt het dronetijdperk in
Grootste politiemacht in de VS stapt het dronetijdperk in Is Fe2O3 een sterke elektrolyt of een zwakke elektrolyt?
Is Fe2O3 een sterke elektrolyt of een zwakke elektrolyt?  Wat zijn twee manieren waarop de energie kan worden vastgelegd en gebruikt, hoe beide een huis?
Wat zijn twee manieren waarop de energie kan worden vastgelegd en gebruikt, hoe beide een huis?  Hoeveel atomen zijn er in 4SO2?
Hoeveel atomen zijn er in 4SO2?  Wat is een nevel?
Wat is een nevel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

