
Wetenschap
5 sleutelfactoren die de reactiesnelheid bepalen
Door Michael Judge
Bijgewerkt op 24 maart 2022
In de chemie is de snelheid waarmee een reactie verloopt van cruciaal belang, vooral voor industriële processen. Een reactie die thermodynamisch gunstig maar traag is, zoals de omzetting van diamant in grafiet, kan praktisch nutteloos zijn. Omgekeerd kan een te snelle reactie veiligheidsrisico's met zich meebrengen. Door de factoren die de reactiesnelheid beïnvloeden te begrijpen en te beheersen, kunnen scheikundigen veiligere, efficiëntere processen ontwerpen.
Temperatuur
Het verhogen van de temperatuur versnelt in het algemeen reacties. De onderliggende reden is de activeringsenergiebarrière die moet worden overwonnen voordat moleculen kunnen reageren. Hogere thermische energie verhoogt de kinetische energie van moleculen, zodat meer botsingen de kritische activeringsenergie bereiken. Een bruikbare vuistregel is dat bij veel reacties de snelheid grofweg verdubbelt bij elke temperatuurstijging van 10°C (Arrhenius-gedrag).
Concentratie en druk
Voor reacties in dezelfde fase – bijvoorbeeld twee opgeloste stoffen in water – verhogen hogere concentraties de kans op productieve botsingen, waardoor de reactie wordt versneld. De omvang van het effect hangt af van de volgorde van de reactie met betrekking tot elke reactant. In de gasfase verhoogt het verhogen van de druk op vergelijkbare wijze de botsingsfrequentie, waardoor de reactie vaak wordt versneld in verhouding tot de drukstijging.
Gemiddelde (oplosmiddel)effecten
Het omringende medium kan de reactiesnelheden aanzienlijk veranderen. Oplosmiddelen die geladen of polaire overgangstoestanden stabiliseren, zoals water of zeer polaire organische oplosmiddelen, kunnen de activeringsenergie verlagen en reacties versnellen waarbij ionische tussenproducten betrokken zijn. Omgekeerd kan een niet-polair oplosmiddel een reactie vertragen die een polaire overgangstoestand vereist.
Katalysatoren
Katalysatoren verlagen de activeringsenergie van een reactie door een alternatieve route te bieden. Dit kan de adsorptie van reactanten op een katalytisch oppervlak inhouden, de vorming van tussenliggende complexen of het verschaffen van een georganiseerde omgeving die de overgangstoestand bevordert. Omdat bij een bepaalde temperatuur meer moleculen de lagere energiebarrière bezitten, neemt de totale snelheid toe zonder dat de katalysator wordt verbruikt.
Oppervlak van vaste reagentia
Wanneer één reactant een vaste stof is, beperkt het blootgestelde oppervlak de reactie tot het grensvlak met de andere fase. Het vergroten van het oppervlak – bijvoorbeeld door een vaste stof tot poeder te vermalen – zorgt voor actievere plaatsen en versnelt daardoor de reactie. Klassieke voorbeelden zijn onder meer het sneller roesten van fijn verdeeld ijzer vergeleken met een massief blok.
Door deze factoren strategisch te manipuleren, kunnen scheikundigen de reactiesnelheden verfijnen om te voldoen aan veiligheids-, efficiëntie- en economische doelstellingen.
Hoofdlijnen
- Chimpansees kunnen leren gereedschap te gebruiken zonder anderen te observeren
- Biofysici onthullen hoe drie eiwitten samenwerken om de cellulaire beweging te verfijnen
- Inwoners van Illinois moedigden aan om de eieren van invasieve insecten te vernietigen om de verspreiding te vertragen
- Waarom een vrouwelijk erfgende gen gevonden op het Y -chromosoom?
- Na gametogenese vindt plaats welk proces het diploïde chromosoom aantal soorten voor de volgende generatie herstelt?
- Virussen versus cellen:niet-cellulaire microben begrijpen
- Hoe heet een groep micro -organismen?
- Welke bacteriële vorm kan worden gebogen als een spiraal dik en rigide of dun flexibel?
- Onderzoekers laten zien dat cellen communiceren door gebruik te maken van een glasvezelnetwerk
- De samenstelling van staal uitgelegd:de chemische formule van staal

- Onderzoek naar perovskiet-silicium tandemcellen laat nieuwe weg zien

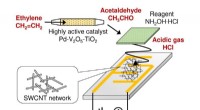
- Ontwikkeling van een kleine sensor die het fytohormoon ethyleen continu kan monitoren
- Eiwitveranderingen gaan vooraf aan foto-isomerisatie van retinale chromofoor
- Gebrouwen koffiedik biedt duurzaam alternatief voor kledingverf

 Welk effect heeft de temperatuur op het diffusieproces?
Welk effect heeft de temperatuur op het diffusieproces?  Onderzoekers simuleren hoe coherente structuren de verwarming van zonnewind beïnvloeden
Onderzoekers simuleren hoe coherente structuren de verwarming van zonnewind beïnvloeden Wat waren de laatste twee planeten in het zonnestelsel en door wie?
Wat waren de laatste twee planeten in het zonnestelsel en door wie?  Wanneer wetenschappers kijken naar Carbon-12 en Carbon-14 Wat weten ze over de atomen?
Wanneer wetenschappers kijken naar Carbon-12 en Carbon-14 Wat weten ze over de atomen?  Kan het vermogen van een robot om te spreken van invloed zijn op het vertrouwen van menselijke gebruikers?
Kan het vermogen van een robot om te spreken van invloed zijn op het vertrouwen van menselijke gebruikers? Leg uit hoe kleur de temperatuur van een ster aangeeft?
Leg uit hoe kleur de temperatuur van een ster aangeeft?  Voordat hij een experiment uitvoert, moet een wetenschapper worden herzien?
Voordat hij een experiment uitvoert, moet een wetenschapper worden herzien?  Nieuwste supercomputer om fusie-energie in internationaal apparaat te helpen ontwikkelen
Nieuwste supercomputer om fusie-energie in internationaal apparaat te helpen ontwikkelen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


