
Wetenschap
Polaire covalente obligaties:definitie, elektronegativiteit en voorbeelden
Hier is een overzicht:
* Covalente binding: Een covalente binding ontstaat wanneer twee atomen een elektronenpaar delen.
* Polair: De term "polair" verwijst naar de ongelijke verdeling van de elektronendichtheid in de binding.
* Elektronegativiteit: Elektronegativiteit is de maatstaf voor het vermogen van een atoom om elektronen aan te trekken in een chemische binding.
Hoe het werkt:
Wanneer twee atomen met verschillende elektronegativiteiten een binding vormen, zal het atoom met de hogere elektronegativiteit de gedeelde elektronen dichter naar zich toe trekken. Hierdoor ontstaat een gedeeltelijke negatieve lading (δ-) op het meer elektronegatieve atoom en een gedeeltelijke positieve lading (δ+) op het minder elektronegatieve atoom.
Voorbeeld:
Beschouw het watermolecuul (H₂O). Zuurstof heeft een hogere elektronegativiteit dan waterstof. Als gevolg hiervan worden de gedeelde elektronen dichter bij het zuurstofatoom getrokken, waardoor het een gedeeltelijk negatieve lading krijgt (δ-). De waterstofatomen, die een gedeeltelijk positieve lading (δ+) hebben, worden aangetrokken door het zuurstofatoom. Hierdoor ontstaat een polaire covalente binding en wordt het watermolecuul als geheel een polair molecuul.
Belangrijkste kenmerken:
* Ongelijke verdeling van elektronen: Elektronen worden niet gelijkelijk verdeeld tussen de atomen.
* Gedeeltelijke kosten: De atomen die bij de binding betrokken zijn, ontwikkelen gedeeltelijk positieve en gedeeltelijk negatieve ladingen.
* Dipoolmoment: Polaire covalente bindingen creëren een dipoolmoment, dat een maat is voor de scheiding van lading binnen een molecuul.
* Oplosbaarheid: Polaire covalente moleculen hebben de neiging oplosbaar te zijn in polaire oplosmiddelen zoals water.
In tegenstelling tot niet-polaire covalente bindingen:
Bij niet-polaire covalente bindingen worden de elektronen gelijkelijk verdeeld tussen de atomen omdat de atomen een vergelijkbare elektronegativiteit hebben. Dit resulteert in geen deelladingen en geen dipoolmoment. Voorbeelden hiervan zijn de bindingen in diatomische moleculen zoals O₂ en N₂.
 Wat is smelt- en kookpunt?
Wat is smelt- en kookpunt?  Welk type molecuul mengt zich het beste met water?
Welk type molecuul mengt zich het beste met water?  Onderzoekers produceren alle RNA-nucleobasen in gesimuleerde oeraardse omstandigheden
Onderzoekers produceren alle RNA-nucleobasen in gesimuleerde oeraardse omstandigheden Welke mineralen lossen op in water?
Welke mineralen lossen op in water?  Een nieuwe methode voor het modelleren van interacties tussen geneesmiddelen en doelwitten herstelt een nadelige vooringenomenheid van technieken uit het verleden
Een nieuwe methode voor het modelleren van interacties tussen geneesmiddelen en doelwitten herstelt een nadelige vooringenomenheid van technieken uit het verleden
 Ontwikkeling kan de impact van de hittegolf verminderen
Ontwikkeling kan de impact van de hittegolf verminderen Een decennium na Deepwater, BP staat voor nieuwe existentiële uitdagingen
Een decennium na Deepwater, BP staat voor nieuwe existentiële uitdagingen Nieuw mechanisme om uit te leggen hoe El Nino het klimaat in Oost-Azië en de NW Pacific beïnvloedt
Nieuw mechanisme om uit te leggen hoe El Nino het klimaat in Oost-Azië en de NW Pacific beïnvloedt Nieuwe analysemethode voor boomringen kan inzichten openen voor het klimaat in het verleden
Nieuwe analysemethode voor boomringen kan inzichten openen voor het klimaat in het verleden Welke 2 criteria gebruiken wetenschappers om levende wezens te classificeren?
Welke 2 criteria gebruiken wetenschappers om levende wezens te classificeren?
Hoofdlijnen
- Nieuwe technieken laten zien hoe microben de gezondheid en biodiversiteit van oceanen bepalen
- Waarom worden ze omega-3-vetzuren genoemd?
- Wat waren voor ons de voor- en nadelen van biotechnologie?
- Wat kan er zijn gebeurd om te voorkomen dat soorten die van dezelfde klasse zijn, ook bij clade behoren?
- Wat is de voetbalvormige structuur die bestaat uit dunne vezels in een scheidingscel?
- Welke stadia van cellulaire ademhaling komen voor in organismen die door anaërobe ademhaling gaan?
- Delen paardenbloemen DNA met mensen?
- Oorsprong van bacteriën:wetenschappelijke hypothesen en theorieën
- Wat is geen belangrijke veronderstelling voor de wetenschappelijke methode?
- Calciumoxalaat oplossen met EDTA:een praktische laboratoriumgids

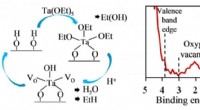
- Niet-vluchtig geheugen zo snel als RAM met de capaciteit van flash
- Een onderzoeksteam ontwikkelt biotransistoren die de kleinste signalen kunnen detecteren

- Grafeenkristallen groeien beter onder koperen afdekking

- Ontdekking van levensverlengingspad in wormen toont nieuwe manier om veroudering te bestuderen
 Een fiets die voor niemand is gebouwd:een fiets zonder bestuurder helpt onderzoekers te leren hoe balans rolt
Een fiets die voor niemand is gebouwd:een fiets zonder bestuurder helpt onderzoekers te leren hoe balans rolt  Welke energie gebruik je voor het runnen van een marathon kinetisch of potentieel?
Welke energie gebruik je voor het runnen van een marathon kinetisch of potentieel?  Nanoscopische streepjescodes stellen een nieuwe wetenschappelijke limiet in
Nanoscopische streepjescodes stellen een nieuwe wetenschappelijke limiet in Informatie voor de werking van cel is gecodeerd in lineaire structuren die worden genoemd?
Informatie voor de werking van cel is gecodeerd in lineaire structuren die worden genoemd?  Hoe de Boeing Dreamliner werkt
Hoe de Boeing Dreamliner werkt  Wat is een geweldige kinderkamer?
Wat is een geweldige kinderkamer?  Stroomopwekking bereikt door een zelf-geassembleerde biobrandstofcel
Stroomopwekking bereikt door een zelf-geassembleerde biobrandstofcel Wat is het netwerk van breedtegraden en lengtes?
Wat is het netwerk van breedtegraden en lengtes?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

