
Wetenschap
Een nieuwe methode voor het modelleren van interacties tussen geneesmiddelen en doelwitten herstelt een nadelige vooringenomenheid van technieken uit het verleden
"Het ontdekken van geneesmiddelen is een zeer lang proces. In elke fase, misschien vindt u uw medicijn niet goed genoeg en moet u een andere kandidaat zoeken, ", legt Xiao-Li Li van A*STAR uit. Zijn team won 'best paper' op de 2016 International Conference on Bioinformatics voor een nieuwe benadering voor het corrigeren van een intrinsiek probleem met machinale leermethoden.
Computer simulatie, of 'in silico'-technieken voor het ontdekken van geneesmiddelen, kan de nauwkeurigheid verbeteren en de uitgerekte, enorm dure weg om een medicijn op de markt te brengen - gemiddeld meer dan 12 jaar en $ 1,8 miljard dollar.
Veel computersimulaties vereisen echter eerst 'training' op datasets van bekende geneesmiddelen en hun doelwitten. Deze gegevens kunnen aanvullende informatie bevatten over de 3D-structuur, chemische samenstelling, en andere moleculaire eigenschappen. Op basis van trends uit deze database met bekende gegevens, de simulatie kan vervolgens de interacties van onbekende moleculen voorspellen, wat leidt tot nieuwe medicijnen en nieuwe doeleiwitten.
Echter, van alle drugs en doelwitten in de database, alleen bepaalde combinaties zullen interageren. Potentiële paren worden ruimschoots gecompenseerd door niet-interagerende paren die 'onbalans tussen klassen' worden genoemd. Verdere onbalans is aanwezig in de vorm van verschillende en ongelijke subtypes van interactie, 'onevenwichtigheid binnen de klas' genoemd.
"Alle rekenmodellen die zijn ontworpen om de nauwkeurigheid te optimaliseren, zijn bevooroordeeld en zullen de neiging hebben om onbekende paren te classificeren in meerderheids- of niet-interactieklasse, " zegt Li. "Meerderheidsklassen zijn beter vertegenwoordigd in gegevens dan minderheidsinteractieklassen - dit vertekent deze modellen en veroorzaakt fouten. Onbalans in gegevens is een uitdagend probleem."
Li's team bij het A*STAR Institute for Infocomm Research, getracht dit te verhelpen door een 'onbalansbewust' algoritme te ontwikkelen dat nauwkeuriger interacties tussen geneesmiddelen voorspelde op basis van een database van 12, 600 bekende interacties en ongeveer 18 miljoen bekende niet-interagerende paren. Het algoritme is ontworpen om ondervertegenwoordigde interactiegroepen beter te herkennen en de gegevens daarin te verbeteren.
Door het verbeteren van het vermogen van het computermodel om zich te concentreren op de meest bruikbare gegevens (de interacties), het team creëerde een systeem dat beter presteerde dan bestaande modelleringstechnieken, nieuwe voorspellen, onbekende geneesmiddel-doelwitinteracties met hoge nauwkeurigheid.
De toekomst van machine learning hangt af van kunstmatige intelligentie en geavanceerd leren, zoals 'deep learning'. Hoe dan ook, zoals Li toevoegt:"data is key. Om ons voorspellend vermogen verder te verbeteren, het eerste wat we kunnen doen is meer relevante gegevens verzamelen over drugs en doelwitten."
 Soorten spectrometers
Soorten spectrometers Peilstoktechnologie kan een revolutie teweegbrengen in de diagnose van ziekten
Peilstoktechnologie kan een revolutie teweegbrengen in de diagnose van ziekten Cryo-EM-structuren van de nicotinereceptor kunnen leiden tot nieuwe therapieën voor verslaving
Cryo-EM-structuren van de nicotinereceptor kunnen leiden tot nieuwe therapieën voor verslaving Structureel bewijs voor een dynamische metallocofactor tijdens distikstofreductie door Mo-nitrogenase
Structureel bewijs voor een dynamische metallocofactor tijdens distikstofreductie door Mo-nitrogenase Onderzoekers identificeren een psychedelisch-achtig medicijn zonder de hallucinogene bijwerkingen
Onderzoekers identificeren een psychedelisch-achtig medicijn zonder de hallucinogene bijwerkingen
 Extra 100 miljoen jaar voordat de aarde permanent zuurstof zag stijgen
Extra 100 miljoen jaar voordat de aarde permanent zuurstof zag stijgen Dieren stierven in giftige soep tijdens de ergste massa-extinctie op aarde:een waarschuwing voor vandaag
Dieren stierven in giftige soep tijdens de ergste massa-extinctie op aarde:een waarschuwing voor vandaag Nieuwe studie meet UV-filters in zeewater en koralen uit Hawaii
Nieuwe studie meet UV-filters in zeewater en koralen uit Hawaii Lijst met gereedschappen en wapens van Stone
Lijst met gereedschappen en wapens van Stone Finland hoopt klimaatbelofte veilig te stellen als EU-leider
Finland hoopt klimaatbelofte veilig te stellen als EU-leider
Hoofdlijnen
- 5 stadia van mitose
- Wetenschappers afluisteren onbekende spitssnuitdolfijnen af om te zien hoe diep ze duiken
- Hoe reproduceren protisten?
- Nieuwe slangensoort verstopt zich in het volle zicht
- Hoe fotosynthese licht vangt en het leven op aarde aandrijft
- Definieer Contrast in microscopen
- De verbazingwekkende efficiëntie van het leven
- Wat gebeurt er met een diercel wanneer deze zich in een hypotone oplossing bevindt?
- Oncogene: wat is het? & Hoe beïnvloedt het de celcyclus?
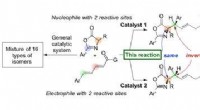
- Bepaal de creatie van chiraliteit door organische katalysatoren
- Materiaalchemici tappen lichaamswarmte af om slimme kleding van stroom te voorzien

- Goedkopere waterstofproductie

- Forensisch onderzoek van FBI bereikt snelheid in Hollywood, onderzoeker zegt:

- Ontkoppeling van elektronisch en thermisch transport

 DOJ praat met staten in brede tech antitrust-sonde
DOJ praat met staten in brede tech antitrust-sonde In het oog springende raciale verschillen in buitenschoolse schorsingen, een waarschuwing over de rol van wetshandhaving ter plaatse
In het oog springende raciale verschillen in buitenschoolse schorsingen, een waarschuwing over de rol van wetshandhaving ter plaatse Nieuwe theorie stuurt temperaturen naar nieuwe dieptepunten
Nieuwe theorie stuurt temperaturen naar nieuwe dieptepunten atalhöyük:9, 000 jaar geleden, een gemeenschap met moderne stedelijke problemen
atalhöyük:9, 000 jaar geleden, een gemeenschap met moderne stedelijke problemen Hoe maak je een ecosysteem voor kinderen met pop-flessen
Hoe maak je een ecosysteem voor kinderen met pop-flessen Onderzoekers stemmen optische en fotokatalytische eigenschappen van C-dots af
Onderzoekers stemmen optische en fotokatalytische eigenschappen van C-dots af Campylobacter gebruikt andere organismen als Trojaans paard om nieuwe gastheren te infecteren
Campylobacter gebruikt andere organismen als Trojaans paard om nieuwe gastheren te infecteren Het verschil tussen sanering en interventie in de wiskunde
Het verschil tussen sanering en interventie in de wiskunde
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

