
Wetenschap
Fluor versus jodium:verschillen in reactiviteit begrijpen
1. Kleinere atoomgrootte: Fluor is veel kleiner dan jodium. Dit betekent dat de elektronen in de buitenste schil dichter bij de kern zitten en een sterkere aantrekkingskracht ervaren. Dit maakt het voor fluor gemakkelijker om een elektron te verkrijgen en een negatief ion te vormen.
2. Hogere elektronegativiteit: Fluor heeft de hoogste elektronegativiteit van alle elementen. Dit betekent dat het een sterke aantrekkingskracht uitoefent op gedeelde elektronen in een binding. Hierdoor is de kans groter dat fluor elektronen van andere atomen aantrekt, wat leidt tot bindingsvorming.
3. Zwakkere elektron-elektronafstoting: Met een kleinere atoomstraal ervaren de elektronen in de buitenste schil van fluor minder afstoting van elkaar. Dit maakt het voor fluor gemakkelijker om een extra elektron aan te trekken.
4. Afwezigheid van d-orbitalen: Fluor, dat zich in de tweede periode bevindt, mist d-orbitalen. Dit beperkt het vermogen om zijn valentieschil uit te breiden, waardoor de kans groter wordt dat het een enkele binding vormt. Jodium kan, vanwege zijn grotere omvang en aanwezigheid van d-orbitalen, meerdere bindingen vormen.
5. Dissociatie-energie van lagere bindingen: De binding tussen fluoratomen is zwakker dan de binding tussen jodiumatomen. Dit maakt het gemakkelijker om de fluor-fluorbinding te verbreken en nieuwe bindingen met andere elementen te vormen.
Samengevat:
De kleinere omvang van fluor, de hogere elektronegativiteit, de zwakkere elektron-elektronenafstoting, de afwezigheid van d-orbitalen en de lagere dissociatie-energie van bindingen dragen allemaal bij aan de hoge reactiviteit ervan in vergelijking met jodium. Deze factoren maken het voor fluor gemakkelijker om elektronen te verkrijgen, bindingen te vormen en deel te nemen aan chemische reacties.
 Welke kleur zal een kobaltchloridepapier veranderen als er waterdamp is?
Welke kleur zal een kobaltchloridepapier veranderen als er waterdamp is?  Wat is het product van Sn-HCl?
Wat is het product van Sn-HCl?  poreuze TPMS-structuren:van ontwerp op meerdere schalen en nauwkeurige additieve fabricage tot multidisciplinaire toepassingen
poreuze TPMS-structuren:van ontwerp op meerdere schalen en nauwkeurige additieve fabricage tot multidisciplinaire toepassingen Tussen beryllium en barium zal welk element de lagere ionisatie -energie hebben?
Tussen beryllium en barium zal welk element de lagere ionisatie -energie hebben?  Wat is de samenstelling van doloston?
Wat is de samenstelling van doloston?
 Zuid-Frankrijk gaat bruisen door klimaatverandering
Zuid-Frankrijk gaat bruisen door klimaatverandering Epische droogte betekent watercrisis aan de grens tussen Oregon en Californië
Epische droogte betekent watercrisis aan de grens tussen Oregon en Californië NASA brengt nieuwe, gedetailleerde Groenlandse gletsjergegevens
NASA brengt nieuwe, gedetailleerde Groenlandse gletsjergegevens Enorme aardbeving in Bolivia onthult bergen 660 kilometer onder onze voeten
Enorme aardbeving in Bolivia onthult bergen 660 kilometer onder onze voeten Bredere dekking van satellietgegevens detecteert de aanvoer van magma naar vulkanen beter
Bredere dekking van satellietgegevens detecteert de aanvoer van magma naar vulkanen beter
Hoofdlijnen
- Wat zal GLAST ons vertellen?
- Wat is een voorbeeld van de functie nerveus weefsel?
- Zure druiven:Besschade, fruitvliegjes verergeren wijn
- Lichtshow in levende cellen:nieuwe methode maakt gelijktijdige fluorescerende labeling van veel eiwitten mogelijk
- Grote eiwitten van het bloed- en lichaamsvloeistoffen geproduceerd door het immuunsysteem in reactie op invasie buitenlandse moleculen?
- Welke tak van biologie gaat over de aardveroudering?
- Vergelijk en vergelijk DNA & RNA
- Wat is het proces van welke organismen nakomelingen produceren om hun soort te bestendigen?
- Genetische klokken bij zoöplanktonsoorten reguleren wat waarschijnlijk de grootste dagelijkse beweging van biomassa ter wereld is
- Koffiecreamer in poedervorm:het onverwachte brandgevaar in de buurt van keukenvlammen

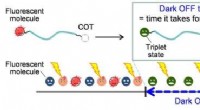
- Wanneer FRETing over kankerbiomarkers niet zal werken, focus in plaats daarvan op knipperen
- Recycling en hergebruik van versleten kathoden om nieuwe lithium-ionbatterijen te maken

- Weg van plastic:het geval van solid body wash

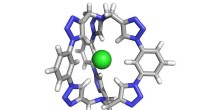
- Een betere zoutvanger bouwen:wetenschappers synthetiseren een moleculaire kooi om chloride op te vangen
 Wat is het toestandssymbool voor natriumchloride -oplossing?
Wat is het toestandssymbool voor natriumchloride -oplossing?  Wat zijn de verschillende soorten windenergie?
Wat zijn de verschillende soorten windenergie?  Wat moet een cel van eukaryote DNA vasthouden die prokaryote niet heeft?
Wat moet een cel van eukaryote DNA vasthouden die prokaryote niet heeft?  Het Russische Novatek kondigt de lancering aan van een enorm Arctisch gasproject
Het Russische Novatek kondigt de lancering aan van een enorm Arctisch gasproject Kunstmatige intelligentie detecteert ongedierte in trailcams en volgt inheemse planten vanuit de ruimte
Kunstmatige intelligentie detecteert ongedierte in trailcams en volgt inheemse planten vanuit de ruimte Wat maakt gebruik van waterkracht?
Wat maakt gebruik van waterkracht?  ATLAS Experiment lanceert nieuwe zoektocht naar langlevende deeltjes
ATLAS Experiment lanceert nieuwe zoektocht naar langlevende deeltjes Work How Caterpillar schrankladers en multi-terrain
Work How Caterpillar schrankladers en multi-terrain
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

