
Wetenschap
Berekening van de productopbrengst bij chemische reacties:een gids voor stoichiometrie
* Chemische reacties en stoichiometrie: Chemische reacties volgen specifieke verhoudingen van reactanten en producten. Deze verhouding wordt bepaald door de uitgebalanceerde chemische vergelijking voor de reactie.
* De evenwichtige vergelijking: De coëfficiënten in een uitgebalanceerde chemische vergelijking vertegenwoordigen het aantal mol van elke betrokken stof.
* Mollen en massa: Om de massa van reactanten te relateren aan de massa van producten, moet je grammen naar mol omrekenen met behulp van de molaire massa van elke stof.
Dit is wat u moet weten om dit probleem op te lossen:
1. De gebalanceerde chemische vergelijking: Dit vertelt u de molverhouding tussen de reactant en het product.
2. De molaire massa van de reactant: Dit zet gram reactant om in mol reactant.
3. De molaire massa van het product: Hiermee worden mol product omgezet in gram product.
Voorbeeld:
Laten we zeggen dat de reactie is:
2H₂ + O₂ → 2H₂O
Dit betekent dat voor elke 2 mol waterstof (H₂) die reageert met 1 mol zuurstof (O₂), je 2 mol water (H₂O) produceert.
Stappen om de productmassa te berekenen:
1. Convert gram reactant om in mol:
- Deel de massa van de reactant (4 gram) door zijn molaire massa.
2. Gebruik de molverhouding uit de uitgebalanceerde vergelijking:
- Bepaal het aantal geproduceerde mol product op basis van de molverhouding in de uitgebalanceerde vergelijking.
3. Mollen product omrekenen naar grammen:
- Vermenigvuldig het aantal mol product met de molaire massa.
Laat me weten of u het volgende kunt verstrekken, zodat ik u kan helpen de productmassa te berekenen:
* De uitgebalanceerde chemische vergelijking voor de reactie.
* De identiteit van de reactant (zodat we de molaire massa ervan kunnen vinden).
* De identiteit van het product (zodat we de molaire massa ervan kunnen vinden).
 Berggletsjers krimpen over het westen
Berggletsjers krimpen over het westen Wat voor zinnen kunt u maken met het woord ecologie?
Wat voor zinnen kunt u maken met het woord ecologie?  De grootste spinnen in Virginia
De grootste spinnen in Virginia Hoe soorten ontstaan:wat de verwarde geschiedenis van de relaties tussen ijsbeer en bruine beer ons vertelt
Hoe soorten ontstaan:wat de verwarde geschiedenis van de relaties tussen ijsbeer en bruine beer ons vertelt  Virtuele hekken en vee:hoe nieuwe technologie effectieve, duurzaam land delen
Virtuele hekken en vee:hoe nieuwe technologie effectieve, duurzaam land delen
Hoofdlijnen
- Vliegenjager heeft 30 nieuwe soorten beschreven
- Wat betekenen gegevens in een experiment?
- Tropische en woestijngrassen kunnen verder naar het zuiden migreren
- Wat is een voorbeeld van het kenmerk om te groeien en te ontwikkelen?
- Hoed wordt de specifieke naam gegeven aan organismen?
- Enzymactiviteit in appels
- Wat betekent biofocaal?
- Verschillen tussen lichaamscellen en neuronen
- Als ik honderden Australiërs vroeg of ze insecten zouden eten, zeiden de meesten ja, dus wat houdt mensen tegen?
- Moleculair magnetisme combineert kracht met boodschapperelektron

- Onderzoekers ontwikkelen nieuwe chip voor superieure forensische detectie van bloedresten

- De slingpsychrometer onder de knie krijgen:stapsgewijze handleiding voor het meten van de vochtigheid en het dauwpunt

- Butanol in latexverf gedetecteerd door massaspectrometrietechnologie
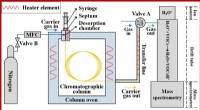
- Ontwerpen van synthetische materialen op natuurlijke basis

 Gebruik de termen oplosmiddel en opgeloste stof om te beschrijven hoe je een zoutoplossing bereidt?
Gebruik de termen oplosmiddel en opgeloste stof om te beschrijven hoe je een zoutoplossing bereidt?  Is de frequentie van de blokgolf gelijk aan de baudsnelheid?
Is de frequentie van de blokgolf gelijk aan de baudsnelheid?  DNA- en RNA-virussen:viraal genetisch materiaal begrijpen
DNA- en RNA-virussen:viraal genetisch materiaal begrijpen  Chemische reacties:de transformatie van stoffen begrijpen
Chemische reacties:de transformatie van stoffen begrijpen  Waarom moet ammoniak worden gedroogd vóór een reactie met natrium?
Waarom moet ammoniak worden gedroogd vóór een reactie met natrium?  Wat gebeurt er als u een geologisch aggregaat van mineralen combineert met de laagste vorm?
Wat gebeurt er als u een geologisch aggregaat van mineralen combineert met de laagste vorm?  Nieuw onderzoek onthult effect van opwarming van de aarde op het smelten van Groenlandse ijs
Nieuw onderzoek onthult effect van opwarming van de aarde op het smelten van Groenlandse ijs Studie onderzoekt hoe klimaatverandering de regen in de Amerikaanse Corn Belt kan beïnvloeden
Studie onderzoekt hoe klimaatverandering de regen in de Amerikaanse Corn Belt kan beïnvloeden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

