
Wetenschap
Meerdere covalente obligaties:definitie, typen en voorbeelden
* Covalente binding: Een binding die ontstaat wanneer twee atomen elektronen delen.
* Meerdere: Verwijst naar het delen van *meer dan één* elektronenpaar.
* Typen:
* Dubbele obligatie: Twee atomen delen twee elektronenparen (in totaal vier elektronen). Weergegeven door twee lijnen die de atomen in een chemische structuur verbinden.
* Triple Bond: Twee atomen delen drie elektronenparen (in totaal zes elektronen). Weergegeven door drie lijnen die de atomen in een chemische structuur verbinden.
Voorbeelden:
* Zuurstof (O2): Zuurstofatomen vormen een dubbele binding om een stabiel octet te bereiken.
* Stikstof (N2): Stikstofatomen vormen een drievoudige binding om een stabiel octet te bereiken.
* Kooldioxide (CO2): Koolstof vormt dubbele bindingen met elk zuurstofatoom.
Eigenschappen van meerdere covalente obligaties:
* Sterkere banden: Meerdere bindingen zijn over het algemeen sterker dan enkele bindingen omdat er meer elektronen worden gedeeld, wat leidt tot een grotere elektrostatische aantrekkingskracht tussen de atomen.
* Kortere bindingslengte: Door de sterkere aantrekkingskracht worden de atomen dichter bij elkaar gehouden.
* Hogere bindingsenergie: Er is meer energie nodig om meerdere bindingen te verbreken dan voor enkele bindingen.
Samengevat: Meerdere covalente bindingen zijn cruciaal voor de stabiliteit en functionaliteit van veel moleculen en dragen bij aan hun unieke eigenschappen en chemische reactiviteit.
 Wanneer een minerial wordt gemalen in poeder, is dit de kleur van soms niet hetzelfde AD origineel mineraal?
Wanneer een minerial wordt gemalen in poeder, is dit de kleur van soms niet hetzelfde AD origineel mineraal?  Ontwikkeld multivalent zelf-geassembleerd bindereiwit tegen SARS-CoV-2 RBD
Ontwikkeld multivalent zelf-geassembleerd bindereiwit tegen SARS-CoV-2 RBD Wat ontstaat er als zwavel en zuurstof gecombineerd worden?
Wat ontstaat er als zwavel en zuurstof gecombineerd worden?  Zuurgraad of alkaliteit (pH) meten – een stapsgewijze handleiding
Zuurgraad of alkaliteit (pH) meten – een stapsgewijze handleiding  Hoe een zuur neutraliseren
Hoe een zuur neutraliseren
 NASA's Terra Satellite vangt het einde van de tropische depressie Kulap
NASA's Terra Satellite vangt het einde van de tropische depressie Kulap Als de verwarming aan is, we hebben stadsbrede plannen nodig om koel te blijven
Als de verwarming aan is, we hebben stadsbrede plannen nodig om koel te blijven LSU helpt bij het bestrijden van invasieve wateronkruid in Puerto Rico
LSU helpt bij het bestrijden van invasieve wateronkruid in Puerto Rico Onderzoekers vinden betrouwbare gegevens over klimaatverandering in nabijgelegen koralen
Onderzoekers vinden betrouwbare gegevens over klimaatverandering in nabijgelegen koralen Nederlanders trekken voor de dooi hun schaatsen aan in Amsterdam
Nederlanders trekken voor de dooi hun schaatsen aan in Amsterdam
Hoofdlijnen
- Nieuwe functies voor 'junk'-DNA?
- Welke baan heeft een kern?
- Wat is een symbiotische relatie waarin het ene organisme ten goede komt aan het andere dat niet wordt beïnvloed?
- Hoe zijn de verdeeldheid tussen cellen in veel schimmels genaamd-?
- Het cluster van het ontwikkelen van cellen van conceptie tot de geboorte wordt een.?
- Wat is genetisch materiaal welke organismen van hun ouders erven?
- Hoe krijgen wetenschappers informatie?
- Wat is de werkelijke grootte van mitochondriën?
- Hyfen die horizontaal groeien langs het oppervlak van een voedselbron worden genoemd?
- Kleding maken van melk

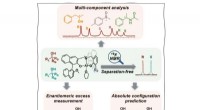
- Fluor maakt scheidingsvrije chirale chromatografische analyse mogelijk
- We hebben in minuten zonder hitte diamanten gemaakt door de kracht van een asteroïdebotsing na te bootsen
- Gevonden:de heilige graal van katalyse:methaan omzetten in methanol onder omgevingsomstandigheden met behulp van licht

- Kristaleilanden kunnen de tijd en kosten van wetenschappelijke experimenten halveren

 Wat zijn de energietransfers van een elektrische ventilator?
Wat zijn de energietransfers van een elektrische ventilator?  Een touw op nanoschaal, en weer een stap in de richting van complexe nanomaterialen die zichzelf assembleren
Een touw op nanoschaal, en weer een stap in de richting van complexe nanomaterialen die zichzelf assembleren Hoe zou de hemel verschijnen in afwezigheid van de atmosfeer van de aarde?
Hoe zou de hemel verschijnen in afwezigheid van de atmosfeer van de aarde?  Bereken de dichtheid van een polymeermengsel
Bereken de dichtheid van een polymeermengsel Wat zijn de twee belangrijkste componenten van fotosynthese?
Wat zijn de twee belangrijkste componenten van fotosynthese?  Waar was Antarctica gevestigd in het Super Continent -leeftijd?
Waar was Antarctica gevestigd in het Super Continent -leeftijd?  De belangrijkste minerale hulpbronnen van Rusland:een uitgebreid overzicht
De belangrijkste minerale hulpbronnen van Rusland:een uitgebreid overzicht  Versnelde analyse van de stabiliteit van complexe legeringen
Versnelde analyse van de stabiliteit van complexe legeringen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

