
Wetenschap
Gedelokaliseerde Pi-obligaties:definitie, voorbeelden en belang
1. Aromatische verbindingen:
* Benzeen: Het klassieke voorbeeld. De zes koolstofatomen vormen een ring met afwisselend enkele en dubbele bindingen. De pi-elektronen zijn echter niet beperkt tot deze individuele bindingen, maar zijn gedelokaliseerd over de hele ring, waardoor een stabiele, vlakke structuur ontstaat.
* Andere aromatische systemen: Naftaleen, antraceen, pyridine, furaan, thiofeen, enz. vertonen allemaal een vergelijkbare delokalisatie van hun pi-elektronen binnen hun ringsystemen.
2. Geconjugeerde systemen:
* Polyenen: Moleculen met afwisselend enkele en dubbele bindingen. De pi-elektronen zijn gedelokaliseerd over het gehele geconjugeerde systeem, waardoor ze stabieler zijn dan geïsoleerde dubbele bindingen.
* Carbonylverbindingen: Aldehyden en ketonen hebben een pi-binding tussen de koolstof- en zuurstofatomen. Deze pi-binding kan worden gedelokaliseerd in aangrenzende enkele bindingen als de carbonylgroep is verbonden met een dubbele binding of een systeem van geconjugeerde dubbele bindingen.
3. Bepaalde ionen:
* Carboxylaatanionen: De negatieve lading in carboxylaten wordt gedelokaliseerd over beide zuurstofatomen, wat resulteert in een resonantie hybride structuur.
* Nitraatanionen: De negatieve lading wordt over alle drie de zuurstofatomen verspreid.
4. Metaalcomplexen:
* Liganden: Sommige liganden, zoals cyclopentadienyl (Cp), kunnen gedelokaliseerde pi-bindingen vormen met metaalatomen in organometaalverbindingen.
Belangrijkste kenmerken van gedelokaliseerde Pi-obligaties:
* Verhoogde stabiliteit: Gedelokaliseerde pi-bindingen zijn over het algemeen stabieler dan gelokaliseerde pi-bindingen vanwege de verhoogde elektronendichtheid in het systeem.
* Lagere energie: De delokalisatie van elektronen verlaagt de totale energie van het molecuul.
* Verbeterde reactiviteit: Gedelokaliseerde pi-bindingen kunnen deelnemen aan verschillende reacties, waaronder elektrofiele aromatische substitutie, nucleofiele additie en Diels-Alder-reacties.
Het begrijpen van het concept van gedelokaliseerde pi-bindingen is cruciaal voor het begrijpen van de structuur, eigenschappen en reactiviteit van een breed scala aan organische en anorganische moleculen.
 Parijs bestelt 800 nieuwe elektrische bussen om smog te bestrijden
Parijs bestelt 800 nieuwe elektrische bussen om smog te bestrijden Lava gutst uit vulkaan bij Manilla; tienduizenden vluchten
Lava gutst uit vulkaan bij Manilla; tienduizenden vluchten Stapstenen voor wilde dieren:hoe het verbinden van geïsoleerde habitats de natuur in onze steden kan helpen bloeien
Stapstenen voor wilde dieren:hoe het verbinden van geïsoleerde habitats de natuur in onze steden kan helpen bloeien  Satellietgegevens tonen verlies van sneeuwbedekking, niet roet verantwoordelijk voor snelle temperatuurstijging in het noordpoolgebied
Satellietgegevens tonen verlies van sneeuwbedekking, niet roet verantwoordelijk voor snelle temperatuurstijging in het noordpoolgebied Wanneer wordt de wetenschappelijke methode belangrijk voor ons?
Wanneer wordt de wetenschappelijke methode belangrijk voor ons?
Hoofdlijnen
- Welk type RNA is de transcriptie van het eindproduct?
- Wat kunnen de fenotypes zijn van twee organismen die verschillende genotypen hebben gevonden, maar hetzelfde fenotype?
- Belangrijke vondst laat zien hoe genregulatoren verschillende partners selecteren om organen te vormen
- Stappen voor het succesvol telen van zoete aardappelen in Washington
- Hoe werken groepen organen samen?
- Plankton zwemt tegen de stroom in
- Waarom is cellulaire ademhaling belangrijk voor de biosfeer?
- Wat zijn 2 structuren die binnen de kern worden gevonden?
- Zouden dierencellen normaal gesproken aan elkaar worden bevestigd?
- Nieuw onderzoek kan leiden tot meer behandelingsopties voor diabetespatiënten
- Dit computerprogramma maakt farmaceutische patenten luchtdicht
- Onderzoekers melden doorbraak in ijsafstotende materialen

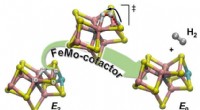
- Chemici onthullen één mechanisme van diwaterstofproductie door stikstofase
- Kaas maken is afhankelijk van melkeiwitten om structuur te vormen

 Wat stuurt stromend water door een turbine die generator draait om elektriciteit te creëren?
Wat stuurt stromend water door een turbine die generator draait om elektriciteit te creëren?  Het gebruik van materiaal met een hoge energiedichtheid in het ontwerp van de elektrode verbetert lithiumzwavelbatterijen
Het gebruik van materiaal met een hoge energiedichtheid in het ontwerp van de elektrode verbetert lithiumzwavelbatterijen Waarom is zilvernitraatoplossing onstabiel?
Waarom is zilvernitraatoplossing onstabiel?  Waarom is graniet gemakkelijker schoon te reinigen dan kalksteen?
Waarom is graniet gemakkelijker schoon te reinigen dan kalksteen?  Wat is de oorsprong van iridium?
Wat is de oorsprong van iridium?  Welke hoeveelheid neerslag definieert een woestijnbioom?
Welke hoeveelheid neerslag definieert een woestijnbioom?  Lucas sluit een lamp aan in de muur. De gloeilamp om bochten. Wat voor soort energietransformatie is dit?
Lucas sluit een lamp aan in de muur. De gloeilamp om bochten. Wat voor soort energietransformatie is dit?  Tropische storm Elsa komt aan land, gaat naar Georgië
Tropische storm Elsa komt aan land, gaat naar Georgië
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

