
Wetenschap
Intermoleculaire krachten begrijpen:vloeistoffen versus vaste stoffen
* Vloeistoffen:
* Sterkere intermoleculaire krachten vergeleken met gassen. Dit is de reden waarom vloeistoffen een bepaald volume hebben, maar geen bepaalde vorm.
* Intermoleculaire krachten worden overwonnen door thermische energie , waardoor moleculen vrij in de vloeistof kunnen bewegen.
* Vaste stoffen:
* Zeer sterke intermoleculaire krachten , die moleculen in een vaste, stijve structuur houden. Dit geeft vaste stoffen hun definitieve vorm en volume.
* Thermische energie is onvoldoende om de sterke intermoleculaire krachten te overwinnen, zodat moleculen in vaste stoffen voornamelijk rond vaste posities trillen.
Soorten intermoleculaire krachten:
1. Waterstofbinding: Een bijzonder sterk type dipool-dipool-interactie die optreedt tussen een waterstofatoom gebonden aan een zeer elektronegatief atoom (zoals zuurstof, stikstof of fluor) en een elektronenpaar op een nabijgelegen elektronegatief atoom.
2. Dipool-dipool-interacties: Komt voor tussen polaire moleculen die een permanent positief en negatief uiteinde hebben (dipool). Deze dipolen richten zich zo op dat het positieve uiteinde van het ene molecuul wordt aangetrokken door het negatieve uiteinde van het andere.
3. Verspreidingskrachten in Londen: Dit zijn zwakke, tijdelijke krachten die voortkomen uit tijdelijke fluctuaties in de elektronendichtheid rond een molecuul. Deze fluctuaties creëren tijdelijke dipolen, die dipolen in aangrenzende moleculen induceren. Ze komen voor tussen alle moleculen, inclusief niet-polaire moleculen.
4. Ionische krachten: Komt voor in ionische verbindingen, waar er een sterke elektrostatische aantrekkingskracht bestaat tussen tegengesteld geladen ionen. Deze krachten zijn het sterkste type intermoleculaire kracht.
Samengevat: De sterkte van de intermoleculaire krachten bepaalt de toestand van de materie. Sterke intermoleculaire krachten zijn verantwoordelijk voor de stijfheid van vaste stoffen, terwijl zwakkere intermoleculaire krachten de vloeibaarheid van vloeistoffen mogelijk maken.
 Hoeveel waterstofatomen zitten er in methyl?
Hoeveel waterstofatomen zitten er in methyl?  Het potentieel van niet-giftige materialen om lood in perovskietzonnecellen te vervangen
Het potentieel van niet-giftige materialen om lood in perovskietzonnecellen te vervangen Wetenschappers ontdekken nieuwe klasse van halfgeleidende entropie-gestabiliseerde materialen
Wetenschappers ontdekken nieuwe klasse van halfgeleidende entropie-gestabiliseerde materialen Waar of niet waar Water is een voorbeeld van een polair molecuul?
Waar of niet waar Water is een voorbeeld van een polair molecuul?  Hoe kan een leerling een magneet gebruiken om aan te geven dat het combineren van ijzer en zwavel een mengsel van en fysieke verandering teweegbrengt?
Hoe kan een leerling een magneet gebruiken om aan te geven dat het combineren van ijzer en zwavel een mengsel van en fysieke verandering teweegbrengt?
 Overstroming in Texas:onderzoekers vergelijken vervuilingsniveaus voor en na orkaan Harvey
Overstroming in Texas:onderzoekers vergelijken vervuilingsniveaus voor en na orkaan Harvey NASA observeert zware moessonregens in Sri Lanka
NASA observeert zware moessonregens in Sri Lanka Drie voorbeelden van puntbronverontreinigende stoffen
Drie voorbeelden van puntbronverontreinigende stoffen  In wetenschappelijk onderzoek dat een observatie doet, leidt het meestal tot?
In wetenschappelijk onderzoek dat een observatie doet, leidt het meestal tot?  Schimmelmuggen:identificatie, impact en effectieve controlemethoden
Schimmelmuggen:identificatie, impact en effectieve controlemethoden
Hoofdlijnen
- Welke organismen produceren hun eigen voedsel?
- Relatie tussen DNA-basen Genen, eiwitten en eigenschappen
- Wie heeft het woord noggin uitgevonden?
- Organismen die zijn verdeeld in klassen die worden genoemd?
- Wat is het verschil tussen ribozym en enzym?
- Wat is de betekenis van chromosoomnummer in gameten?
- Wat hondeneigenaren moeten weten over leptospirose
- Hoe zou je de functie van het voortplantingssysteem omschrijven?
- Hoe zijn zowel weefselorganen als orgaansystemen anders?
- Nieuw type elektrolyt kan de prestaties van supercondensatoren verbeteren

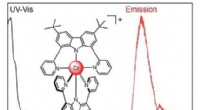
- Een nieuw chroomcomplex zendt licht uit in de ongrijpbare NIR-II-golflengte
- Video:De chemie van gebakken kip

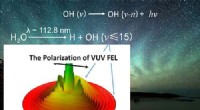
- Studie onthult fotolyse van water en de bijdragen ervan aan hydroxyl-daggloedemissies in de atmosfeer van de aarde en Mars
- Sproeidrogen om nieuwe materialen te produceren in industriële toepassingen

 Wat is het totale aantal bezette subels in een atoomchloorgrondstaat?
Wat is het totale aantal bezette subels in een atoomchloorgrondstaat?  Hoe kunt u de resultaat van kracht vinden wanneer de richting van 45 graden is gescheiden?
Hoe kunt u de resultaat van kracht vinden wanneer de richting van 45 graden is gescheiden?  Leg uit hoe we weten hoe de binnenkant van de aarde eruit ziet als we er nog nooit zijn geweest?
Leg uit hoe we weten hoe de binnenkant van de aarde eruit ziet als we er nog nooit zijn geweest?  Wat is de onafhankelijke variabele in dit experiment dichter fruit gezonder?
Wat is de onafhankelijke variabele in dit experiment dichter fruit gezonder?  Waar in India werd de geothermische energie gebruikt?
Waar in India werd de geothermische energie gebruikt?  Dynamische compressie biedt nieuw inzicht in het begrijpen en voorspellen van kristalgroei
Dynamische compressie biedt nieuw inzicht in het begrijpen en voorspellen van kristalgroei Wat wordt bedoeld met de wetenschappelijke methode uitgelegd?
Wat wordt bedoeld met de wetenschappelijke methode uitgelegd?  Persoonlijke koelunits in het verschiet
Persoonlijke koelunits in het verschiet
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

