
Wetenschap
De wetten van chemische combinaties begrijpen:een uitgebreide gids
1. Wet van behoud van de massa (Lavoisier, 1789): Deze wet stelt dat in een gesloten systeem de totale massa van de reactanten vóór een chemische reactie gelijk is aan de totale massa van de producten na de reactie. In eenvoudiger bewoordingen kan materie niet worden gecreëerd of vernietigd in een chemische reactie, maar alleen worden getransformeerd.
2. Wet van bepaalde proporties (Proust, 1799): Deze wet stelt dat een bepaalde chemische verbinding altijd dezelfde elementen in dezelfde massaverhouding bevat, ongeacht de bron of bereidingswijze. Water (H₂O) heeft bijvoorbeeld altijd een massaverhouding van 1:8 (ongeveer) voor waterstof tot zuurstof, waar je het ook aantreft.
3. Wet van meervoudige verhoudingen (Dalton, 1803): Deze wet stelt dat wanneer twee elementen meer dan één verbinding vormen, de verhoudingen van de massa's van het ene element in combinatie met de vaste massa van het andere element eenvoudige gehele getallen zijn. Koolstof en zuurstof vormen bijvoorbeeld twee veel voorkomende oxiden:koolmonoxide (CO) en kooldioxide (CO₂). De verhouding zuurstof/koolstof in kooldioxide is tweemaal zo groot als die in koolmonoxide.
4. Wet van de wederzijdse verhoudingen (Richter, 1792): Deze wet stelt dat als twee elementen afzonderlijk combineren met een vaste massa van een derde element, de verhouding van hun massa's waarin ze met elkaar combineren ofwel hetzelfde is, ofwel een eenvoudig veelvoud is van de verhouding waarin ze combineren met het derde element. Dit kan worden gezien als een meer specifieke toepassing van de Wet van Meervoudige Proporties.
5. De wet van Gay-Lussac over het combineren van volumes (Gay-Lussac, 1808): Deze wet is van toepassing op gassen en stelt dat wanneer gassen reageren, ze dit doen in volumes die eenvoudige gehele getalsverhoudingen zijn, ervan uitgaande dat de gassen dezelfde temperatuur en druk hebben. Deze wet leidde, naast de hypothese van Avogadro, tot het inzicht dat gassen uit moleculen bestaan.
Deze wetten hebben, samen met de latere ontwikkeling van de atoomtheorie, de basis gelegd voor ons begrip van hoe materie is gestructureerd en hoe chemische reacties plaatsvinden. Ze zijn nog steeds essentieel voor het begrijpen van de samenstelling en eigenschappen van chemische verbindingen.
 Welke elementen zijn polair en niet -polair?
Welke elementen zijn polair en niet -polair?  Onderzoekers bootsen het gietgedrag van gesmolten metaal na met nieuw ontwikkelde simulatietechnologie
Onderzoekers bootsen het gietgedrag van gesmolten metaal na met nieuw ontwikkelde simulatietechnologie Hoe verankeren stikstofatomen eiwitmoleculen?
Hoe verankeren stikstofatomen eiwitmoleculen?  Is koken de maximale temperatuur die een stof kan bereiken?
Is koken de maximale temperatuur die een stof kan bereiken?  Wie heeft het sterkere dipool-dipool waterstofchloride of flouride?
Wie heeft het sterkere dipool-dipool waterstofchloride of flouride?
 Enorme dooi permafrost kan worden beperkt door ambitieuze klimaatdoelstellingen
Enorme dooi permafrost kan worden beperkt door ambitieuze klimaatdoelstellingen Kunnen parken steden helpen de misdaad te bestrijden?
Kunnen parken steden helpen de misdaad te bestrijden?  Plastic stapelt zich op in Japan na afvalverbod in China:onderzoek
Plastic stapelt zich op in Japan na afvalverbod in China:onderzoek Wetenschappers identificeren twee nieuwe soorten Bagarius-meervallen, waarvan er één tot 220 pond kan wegen
Wetenschappers identificeren twee nieuwe soorten Bagarius-meervallen, waarvan er één tot 220 pond kan wegen  Rocky Mountain-bossen branden nu meer dan ooit in de afgelopen 2, 000 jaar
Rocky Mountain-bossen branden nu meer dan ooit in de afgelopen 2, 000 jaar
Hoofdlijnen
- Wat is het proces in een bepaald meercellig organisme waarmee speciale cellen nieuwe weefsels uit verschillende typen kunnen laten groeien?
- Wat is het verschil tussen levend organisme dood en niet -dingen?
- Wat is prokaryote betekent?
- Nieuwe interactieve technologie maakt zeldzame celtypes zichtbaar
- Wat zijn de transgene bacteriën?
- Hoe een nucleaire aanval op Noord-Korea zou bijdragen aan de mondiale kankerepidemie
- Welke cellen van het lichaam zijn het meest gevoelig voor stralingsschade?
- Wat is de rol van RNA in vertaling?
- Wat zijn niet-autonome transponeerbare elementen in de biologie?
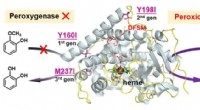
- P450-peroxygenase omzetten in peroxidase via mechanismegestuurde eiwittechnologie
- Moleculaire motor:vier rotatietoestanden
- Shine a light:nieuw onderzoek laat zien hoe energiezuinig licht plastic kan buigen

- Oorsprong van het leven:chemische evolutie in een kleine Golfstroom

- Omzetting van CO2 naar CO op kamertemperatuur:een nieuwe manier om koolwaterstoffen te synthetiseren

 Orbiteren planeten in een cirkel rond de zon?
Orbiteren planeten in een cirkel rond de zon?  Waarom is evolutie een theorie?
Waarom is evolutie een theorie?  Bijna 500 mensen in het zuidoosten van de VS melden meteoor
Bijna 500 mensen in het zuidoosten van de VS melden meteoor Waarom is de hysteresiscurve zo dik in een monster?
Waarom is de hysteresiscurve zo dik in een monster?  Sandia identificeert ongebruikelijke polycyclische aromatische koolwaterstoffen met behulp van tandem-massaspectrometrie
Sandia identificeert ongebruikelijke polycyclische aromatische koolwaterstoffen met behulp van tandem-massaspectrometrie Gemeenschappen moeten samenwerken om te beschermen tegen bosbranden
Gemeenschappen moeten samenwerken om te beschermen tegen bosbranden Hoe nicotine werkt
Hoe nicotine werkt  Hoe berekenen we resulterende krachten?
Hoe berekenen we resulterende krachten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

