
Wetenschap
Ammoniumhydroxide versus natriumhydroxide:de basissterkte begrijpen
Dit is waarom:
* Ammoniumhydroxide is een zwakke base: Het bestaat in evenwicht met ammoniak (NH3 ) en water (H2 O). Slechts een klein deel van de ammoniumhydroxidemoleculen ioniseert daadwerkelijk en vormt hydroxide-ionen (OH - ).
* Natriumhydroxide is een sterke base: Het ioniseert volledig in oplossing, wat betekent dat al zijn moleculen dissociëren in natriumionen (Na + ) en hydroxide-ionen (OH - ).
Daarom produceert natriumhydroxide een veel hogere concentratie hydroxide-ionen in oplossing, waardoor het een veel sterkere base is dan ammoniumhydroxide.
Samenvattend:
* Sterke basis: Volledig ioniseren in oplossing, waardoor een hoge concentratie hydroxide-ionen ontstaat.
* Zwakke basen: Ioniseert slechts gedeeltelijk in oplossing, waardoor een lage concentratie hydroxide-ionen ontstaat.
 Hoe de snelheid van de ontbinding van het gebladerte de koolstofniveaus beïnvloedt
Hoe de snelheid van de ontbinding van het gebladerte de koolstofniveaus beïnvloedt Poll:Amerikanen wijten wild weer aan opwarming van de aarde
Poll:Amerikanen wijten wild weer aan opwarming van de aarde Tropische onweersbuien zullen sterker worden naarmate de wereld warmer wordt
Tropische onweersbuien zullen sterker worden naarmate de wereld warmer wordt Onderzoekers suggereren dat rampen met kolenas en residudammen kunnen worden voorkomen
Onderzoekers suggereren dat rampen met kolenas en residudammen kunnen worden voorkomen Kleine hoogteveranderingen kunnen de impact van de contrail van vluchten tot 59 procent verminderen
Kleine hoogteveranderingen kunnen de impact van de contrail van vluchten tot 59 procent verminderen
Hoofdlijnen
- Door welk proces ook bekend als cel eten is een pacticulaire substantie overspoeld door membraan en vervolgens verteerd?
- Pythons zijn echte chokekunstenaars:grootte alleen verklaart niet hoe ze zulke grote prooien kunnen eten
- Anti-insuline-eiwit gekoppeld aan levensduur en voortplanting bij mieren
- Begrijpen hoe pathogene schimmels hun koolhydraatpantser opbouwen
- Dinosaurussen zwierven ooit door Antarctica:hoe het continent transformeerde van weelderig regenwoud naar bevroren reus
- Wat bevordert de opslag van glucose als glycogeen?
- Wat is de term voor één mogelijke vorm van gen een bepaalde eigenschap?
- Prokaryoten versus eukaryoten:belangrijkste verschillen verklaard
- Welke organismen kunnen worden gedifferentieerd met behulp van een zetmeelagarplaat?
- Wetenschappers ontwikkelen moleculaire thermometer voor contactloze metingen met infraroodlicht

- Een zeer gevoelig en multi-analytisch systeem voor erfelijke nierziekte
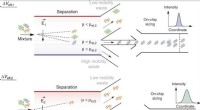
- Microfluidics:2D-vingerafdrukken van heterogene eiwitten in oplossing
- Onderzoekers vinden een manier om het hele spectrum van zonlicht te benutten

- Probiotische hydrogels genezen darmwonden waar andere verbanden niet bij kunnen
 Wat is de hoogte van Stratus -wolken?
Wat is de hoogte van Stratus -wolken?  Duurzame palmolie? Hoe milieubescherming en armoedebestrijding met elkaar verzoend kunnen worden
Duurzame palmolie? Hoe milieubescherming en armoedebestrijding met elkaar verzoend kunnen worden  Enkelwandige koolstofnanobuisjes kunnen dienen als ideale meetpunten om wrijving te bestuderen, smering en slijtage op microschaal
Enkelwandige koolstofnanobuisjes kunnen dienen als ideale meetpunten om wrijving te bestuderen, smering en slijtage op microschaal Onderzoek kijkt naar hoe open source-software wordt geschreven
Onderzoek kijkt naar hoe open source-software wordt geschreven  Wat zijn celstructuren die voedingsmoleculen en oude delen worden afgebroken?
Wat zijn celstructuren die voedingsmoleculen en oude delen worden afgebroken?  Waarom leven dieren in het naaldbos?
Waarom leven dieren in het naaldbos?  Coating op basis van nanodeeltjes voor vliegtuigmotoren kan de levensduur verdrievoudigen en het brandstofverbruik verminderen
Coating op basis van nanodeeltjes voor vliegtuigmotoren kan de levensduur verdrievoudigen en het brandstofverbruik verminderen Wat zou een groot aantal aan het begin van de chemische formule Reprent Ex 3C2?
Wat zou een groot aantal aan het begin van de chemische formule Reprent Ex 3C2?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

