
Wetenschap
Polariteit in de chemie begrijpen:hoe elektronen moleculen vormen
Emilija Randjelovic/iStock/GettyImages
Elektronen in een chemische binding
Wanneer atomen samenkomen, delen ze elektronen die een wolk rond de kernen vormen. Bij covalente bindingen wordt de elektronendichtheid gelijkelijk verdeeld, maar bij polaire bindingen worden de elektronen naar het meer elektronegatieve atoom getrokken, waardoor een lichte onbalans in de lading ontstaat.
Polariteit bepalen
Polariteit hangt af van elektronegativiteit, de aantrekkingskracht die elk atoom uitoefent op gedeelde elektronen. Bereken het elektronegativiteitsverschil:
- 0,4–1,7 →polaire covalente binding
- >1.7→ionisch karakter (elektronen worden overgedragen naar het meer elektronegatieve atoom)
- <0.4→niet-polaire covalente binding (gelijkelijk delen)
Dipoolmoment
Polaire bindingen genereren een dipoolmoment:een negatieve gedeeltelijke lading op het meer elektronegatieve atoom en een positieve gedeeltelijke lading op het andere. De vectorsom van alle bindingsdipolen geeft het netto dipoolmoment van het molecuul weer, wat invloed heeft op eigenschappen zoals de hoge oppervlaktespanning van water.
Polaire versus niet-polaire moleculen
Een molecuul kan polaire bindingen bevatten en toch in het algemeen niet-polair zijn als de dipolen elkaar opheffen. CO₂ heeft bijvoorbeeld twee polaire C–O-bindingen (verschil 1,0), maar de lineaire geometrie maakt de twee dipolen gelijk en tegengesteld, wat een niet-polair molecuul oplevert.
 Waar of niet waar? Stoffen met een pH lager dan 7 zijn zuur?
Waar of niet waar? Stoffen met een pH lager dan 7 zijn zuur?  A functional group changes the structure of a compound but does not alter its chemical properties?
A functional group changes the structure of a compound but does not alter its chemical properties?  Welke elementen hebben 5 elektronen in hun elektronenpuntdiagrammen?
Welke elementen hebben 5 elektronen in hun elektronenpuntdiagrammen?  Welk oxide wordt gebruikt in witte verf?
Welk oxide wordt gebruikt in witte verf?  Noem de toestandsverandering die optreedt wanneer osmium wordt verwarmd van 4000© naar 6000©?
Noem de toestandsverandering die optreedt wanneer osmium wordt verwarmd van 4000© naar 6000©?
Hoofdlijnen
- Wat betekent bacterlurie?
- Welke organen vormen het skeletsysteem?
- Omvatten nucleïnezuren suikers en lipiden?
- Wat doet het ribosoom in een amimale cel?
- Wat zijn de delen van een dierencel?
- Waar in de cel zou je chromosomen vinden?
- Wat zijn de soorten menselijke chromosomen in een karyotype?
- Biologen ontdekken hoe een kankerverwekkend virus de reactie van het immuunsysteem vermijdt
- Waarom is water een biomolecuul?
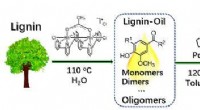
- Nieuwe strategie ontworpen voor duurzame productie van benzylamines uit lignine
- Hooggevoelige nanofotonische sensoren met passieve opsluiting van analytmoleculen in hotspots

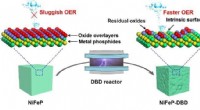
- Etsproces verbetert de extractie van waterstof tijdens elektrolyse van water
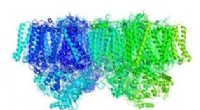
- Mechanisme achter de elektrische ladingen gegenereerd door fotosynthese
- Gigantische omkering van lading voor het eerst waargenomen

 Wat is een hoog soortelijk gewicht?
Wat is een hoog soortelijk gewicht?  Welke temperatuurverandering is nodig voor een vloeistof in vaste stof?
Welke temperatuurverandering is nodig voor een vloeistof in vaste stof?  Watt omrekenen naar kilowattuur:een praktische gids
Watt omrekenen naar kilowattuur:een praktische gids  Vrouwen hebben onderzoek naar vogelzang verstoord, en hun bevindingen laten zien hoe diversiteit alle wetenschapsgebieden kan verbeteren
Vrouwen hebben onderzoek naar vogelzang verstoord, en hun bevindingen laten zien hoe diversiteit alle wetenschapsgebieden kan verbeteren Blijf positief, Scott Morrison:als je mensen uitscheldt voor slecht gedrag, ze doen het meer
Blijf positief, Scott Morrison:als je mensen uitscheldt voor slecht gedrag, ze doen het meer Zwak zuur of basis waarvan de kleur afhankelijk is van de concentratie van hydroniumionen?
Zwak zuur of basis waarvan de kleur afhankelijk is van de concentratie van hydroniumionen?  Gevaar niet voorbij:gaslekken, schimmel weefgetouw voor Harvey evacués
Gevaar niet voorbij:gaslekken, schimmel weefgetouw voor Harvey evacués Welke soort werd het best aangepast aan veranderingen die zich gedurende de langste periode in de omgeving hebben voorgedaan?
Welke soort werd het best aangepast aan veranderingen die zich gedurende de langste periode in de omgeving hebben voorgedaan?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

