
Wetenschap
Ionische versus covalente obligaties:belangrijkste verschillen verklaard
Ionische bindingen:
* Formatie: Ionische bindingen ontstaan wanneer een atoom (meestal een metaal) een of meer elektronen verliest om een positief geladen ion (kation) te worden, terwijl een ander atoom (meestal een niet-metaal) die elektronen krijgt om een negatief geladen ion (anion) te worden. De tegenovergestelde ladingen trekken elkaar vervolgens aan en vormen de binding.
* Elektronenoverdracht: Elektronen worden *overgedragen* van het ene atoom naar het andere.
* Verschil in elektronegativiteit: Er is een groot elektronegativiteitsverschil tussen de atomen (meestal groter dan 1,7) vereist om een ionische binding te vormen.
* Aard van de band: De binding bestaat voornamelijk uit elektrostatische aantrekking tussen de tegengesteld geladen ionen.
* Fysieke eigenschappen: Ionische verbindingen zijn meestal:
* Hoge smelt- en kookpunten door sterke elektrostatische krachten.
* Hard en broos vanwege de stijve roosterstructuur.
* Goede geleiders van elektriciteit wanneer opgelost of gesmolten omdat de ionen vrij kunnen bewegen.
Covalente obligaties:
* Formatie: Covalente bindingen ontstaan wanneer twee atomen een of meer elektronenparen *delen*.
* Elektronen delen: Elektronen worden gedeeld tussen de atomen, waardoor voor beide een stabielere elektronische configuratie ontstaat.
* Verschil in elektronegativiteit: Een kleiner elektronegativiteitsverschil (minder dan 1,7) is kenmerkend voor covalente binding.
* Aard van de band: De binding ontstaat door de wederzijdse aantrekking van de gedeelde elektronen naar de positief geladen kernen van de atomen.
* Fysieke eigenschappen: Covalente verbindingen zijn meestal:
* Lagere smelt- en kookpunten vergeleken met ionische verbindingen.
* Zachter en flexibeler .
* Slechte elektriciteitsgeleiders in vaste en vloeibare toestanden omdat de elektronen zich in de covalente bindingen bevinden.
Overzichtstabel:
| Kenmerk | Ionische binding | Covalente binding |
|------------------|------------|---------------|
| Elektronenoverdracht | Ja | Nee |
| Elektronen delen | Nee | Ja |
| Elektronegativiteitsverschil | Groot | Klein |
| Bondsterkte | Sterk | Variabel |
| Fysieke eigenschappen | Hoog smeltpunt, hard, bros | Lager smeltpunt, zachter, flexibel |
Voorbeeld:
* Ionische binding: Natriumchloride (NaCl) - Natrium verliest een elektron om Na+ te worden en chloor krijgt een elektron om Cl- te worden. De tegengestelde ladingen trekken elkaar aan en vormen een ionische binding.
* Covalente binding: Water (H₂O) - Waterstof en zuurstof delen elektronen om covalente bindingen te vormen.
Opmerking: Het onderscheid tussen ionische en covalente bindingen is niet altijd absoluut. Er zijn gevallen waarin een binding gedeeltelijk ionisch en gedeeltelijk covalent kan zijn, ook wel polaire covalente bindingen genoemd. Dit gebeurt wanneer het elektronegativiteitsverschil niet groot genoeg is om een elektron volledig over te dragen, maar significant genoeg om een gedeeltelijke ladingsscheiding binnen het molecuul te creëren.
 Lijden in de hitte - de toename van mariene hittegolven schaadt oceaansoorten
Lijden in de hitte - de toename van mariene hittegolven schaadt oceaansoorten Naarmate het klimaat warmer wordt, zomermoessons om minder stroom te produceren
Naarmate het klimaat warmer wordt, zomermoessons om minder stroom te produceren Waarom hebben we herfst?
Waarom hebben we herfst?  Je innerlijke alien channelen? Misschien zeggen wetenschappers (update)
Je innerlijke alien channelen? Misschien zeggen wetenschappers (update)  Studie van Darwins vinken werpt licht op hoe één soort tot vele soorten kan leiden
Studie van Darwins vinken werpt licht op hoe één soort tot vele soorten kan leiden
Hoofdlijnen
- Als twee organismen hetzelfde volledige aantal chromosomen hebben, zijn dan altijd ledensoorten?
- Oesters sluiten hun schelpen als reactie op laagfrequente geluiden
- Het stadium van de celcyclus die het meeste leven bezet, is?
- Welke structuur wordt aangetroffen in een plantencel maar afwezig een dierlijke cel?
- Waar gaat deze altijd deel uit van de wetenschappelijke methode?
- Het domein dat echte kernen en membraangebonden organellen omvat?
- Wat zijn de 4 enzymen in DNA -replicatie?
- Is DNA een type enzym dat aminozuur samenstelt om eiwitten te maken?
- Organisme dat binnen of op een ander organisme leeft?
- Nieuwe verbinding kan fotodynamische therapie voor kanker verbeteren

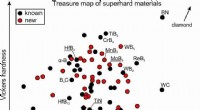
- Alternatieven vinden voor diamanten om te boren
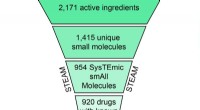
- EEN WOLK aan mogelijkheden:nieuwe therapieën vinden door medicijnen te combineren
- De grenzen van hematiet

- Gerecycleerde bureaustoelen omgetoverd tot hard-shell rugzakken en fietstassen

 Vergeet slimme steden (voor een minuut), we moeten praten over slimme boerderijen
Vergeet slimme steden (voor een minuut), we moeten praten over slimme boerderijen Wat zijn de organismen die samenleven voor wederzijds voordeel?
Wat zijn de organismen die samenleven voor wederzijds voordeel?  Wat is hoogte?
Wat is hoogte?  In het Canadese Quebec waren de bewoners nijdig over de opkomst van de mijnbouw
In het Canadese Quebec waren de bewoners nijdig over de opkomst van de mijnbouw  Welke organel wordt omgeven door twee membranen?
Welke organel wordt omgeven door twee membranen?  Waarom is benzoëzuur beter oplosbaar in een alkalische oplossing dan in een neutrale oplossing?
Waarom is benzoëzuur beter oplosbaar in een alkalische oplossing dan in een neutrale oplossing?  Magnetisme detecteren in atomaire resolutie met slechts een scanning tunneling microscoop
Magnetisme detecteren in atomaire resolutie met slechts een scanning tunneling microscoop Zorgen over hoofdletsel politie
Zorgen over hoofdletsel politie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

