
Wetenschap
Het balanceren van chemische vergelijkingen:de wet van behoud van massa uitgelegd
Hier ziet u hoe het zich verhoudt tot het in evenwicht brengen van chemische vergelijkingen:
* Atomen worden herschikt, niet gemaakt of vernietigd: Chemische reacties omvatten de herschikking van atomen om nieuwe moleculen te vormen. De atomen zelf blijven onveranderd.
* Balanceren zorgt voor gelijke atomen aan beide kanten: Door een chemische vergelijking in evenwicht te brengen, zorg je ervoor dat hetzelfde aantal atomen van elk element verschijnt aan zowel de reactant (uitgangsmaterialen) als de productzijde (resulterende stoffen) van de vergelijking.
* Als weerspiegeling van de wet: Dit evenwicht weerspiegelt het principe van behoud van massa. Omdat je geen atomen kunt creëren of vernietigen, moet de totale massa van de reactanten gelijk zijn aan de totale massa van de producten.
Voorbeeld:
De onevenwichtige vergelijking voor de verbranding van methaan is:
CH₄ + O₂ → CO₂ + H₂O
Deze vergelijking is onevenwichtig omdat:
* Er zijn 4 waterstofatomen aan de linkerkant, maar slechts 2 aan de rechterkant.
* Er zijn 2 zuurstofatomen aan de linkerkant, maar 3 aan de rechterkant.
Om het in evenwicht te brengen, voegen we coëfficiënten toe:
CH₄ + 2 O₂ → CO₂ + 2 H₂O
Nu hebben we:
* 1 koolstofatoom aan beide zijden
* 4 waterstofatomen aan beide zijden
* 4 zuurstofatomen aan beide zijden
Deze uitgebalanceerde vergelijking weerspiegelt de wet van behoud van massa en zorgt ervoor dat de totale massa van de reactanten (methaan en zuurstof) gelijk is aan de totale massa van de producten (kooldioxide en water).
 Het aantal neutronen van waterstof:van protium tot tritium en hun praktische toepassingen
Het aantal neutronen van waterstof:van protium tot tritium en hun praktische toepassingen  Wat zijn de voorbeelden van vaste vloeistof en gas aanwezig in een auto?
Wat zijn de voorbeelden van vaste vloeistof en gas aanwezig in een auto?  Sterke kunstmatige spieren van koolstofvezel kunnen 12 optillen, 600 keer hun eigen gewicht
Sterke kunstmatige spieren van koolstofvezel kunnen 12 optillen, 600 keer hun eigen gewicht Is water zuur na het koken?
Is water zuur na het koken?  Wat is de vergelijking voor de reactie van zout carbonzuur met HCl?
Wat is de vergelijking voor de reactie van zout carbonzuur met HCl?
 Hoe de beweging voor desinvestering van fossiele brandstoffen te corrigeren?
Hoe de beweging voor desinvestering van fossiele brandstoffen te corrigeren? Hoe het geloof in puur kwaad zich verhoudt tot de perceptie en bestraffing van daders van wapengeweld
Hoe het geloof in puur kwaad zich verhoudt tot de perceptie en bestraffing van daders van wapengeweld  Statistieken kunnen ons helpen erachter te komen hoe historische veldslagen anders hadden kunnen aflopen, zeggen experts
Statistieken kunnen ons helpen erachter te komen hoe historische veldslagen anders hadden kunnen aflopen, zeggen experts  Er zijn zelfs microplastics in een uithoek van de Pyreneeën geblazen
Er zijn zelfs microplastics in een uithoek van de Pyreneeën geblazen Welke locatie op aarde krijgt het meeste directe zonlicht?
Welke locatie op aarde krijgt het meeste directe zonlicht?
Hoofdlijnen
- Wat zijn twee dingen gemaakt tijdens cellulaire ademhaling?
- In welke vorm komen eiwitten de cellen van het lichaam binnen?
- Wat maakt een koe een koe? Volledige rundergenoom gesequenced
- Wat is munificatie in biotechnologie?
- Hoe winnen en gebruiken levende organismen massa door de processen van fotosynthese -ademhaling?
- Hoe leren ziekteverwekkers ziekteverwekkers te zijn:partnerschappen tussen microben die ziekten bij de mens leiden
- Wat is een organel dat pakketten wijzigt en materialen uit de cel transporteert?
- Is de natuurlijke en overleving van de sterkste gelijke evolutie?
- Genenstroom bij giraffen en wat dit betekent voor hun behoud
- Opsporen van vuilbronnen voor strafrechtelijk onderzoek
- Screentest voor vingerafdrukken werkt op levenden en overledenen

- Onderzoekers vinden conformationele stoornis die de mobiliteit van ladingsdragers afstemt in 2D-perovskieten

- Nieuwe tool haalt ongrijpbare COVID-19-marker uit menselijk bloed
- Zelfherstellende composieten verlengen de levensduur van een product
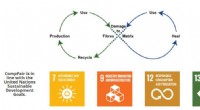
 Hoe heet de vaste plastic mantel?
Hoe heet de vaste plastic mantel?  Welke fusie vindt plaats in het centrum van de zon?
Welke fusie vindt plaats in het centrum van de zon?  Behandeling van ‘back-to-school’-oorinfecties zonder antibioticaresistentie
Behandeling van ‘back-to-school’-oorinfecties zonder antibioticaresistentie  Wat is traangas?
Wat is traangas?  Omdat een object dat in een uniforme cirkelvormige beweging beweegt een constante snelheid aanhoudt, is er geen kracht nodig om het in beweging te houden?
Omdat een object dat in een uniforme cirkelvormige beweging beweegt een constante snelheid aanhoudt, is er geen kracht nodig om het in beweging te houden?  Hebben alfastralen hogere energie dan gammastralen?
Hebben alfastralen hogere energie dan gammastralen?  Wat heeft geen kwestie nodig om energie over te dragen?
Wat heeft geen kwestie nodig om energie over te dragen?  De maan heeft ook fasen waarom we ons denken dat het draait om de zon in plaats van de aarde?
De maan heeft ook fasen waarom we ons denken dat het draait om de zon in plaats van de aarde?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

