
Wetenschap
Dubbele obligaties begrijpen:definitie, voorbeelden en eigenschappen
Hier is een overzicht:
* Covalente binding: Een chemische binding gevormd door het delen van elektronenparen tussen atomen.
* Dubbele binding: Twee elektronenparen worden gedeeld tussen twee atomen.
Voorbeelden:
* Zuurstof (O2): Elk zuurstofatoom deelt twee elektronen met het andere zuurstofatoom, waardoor een dubbele binding ontstaat.
* Kooldioxide (CO2): Elk koolstofatoom vormt een dubbele binding met elk zuurstofatoom.
Belangrijkste kenmerken van dubbele bindingen:
* Sterker dan enkele bindingen: Door het delen van meer elektronen zijn dubbele bindingen sterker en korter dan enkele bindingen.
* Vlakke geometrie: De atomen die betrokken zijn bij een dubbele binding en de atomen die er direct aan vastzitten, liggen meestal in hetzelfde vlak.
* Beperkte rotatie: De rotatie rond een dubbele binding is beperkt, wat leidt tot het bestaan van isomeren (moleculen met dezelfde chemische formule maar met verschillende rangschikkingen van atomen).
Laat het me weten als je meer details wilt over dubbele bindingen of als je andere scheikundige vragen hebt!
Hoofdlijnen
- Wat is wetenschappelijke hypothesen?
- Waarom zijn microscoop nodig om cellen te bestuderen?
- Hoe u kunt profiteren van bioafval
- Wat voor soort vlekken worden gebruikt om cellen te planten en dieren?
- Wat is een evolutionair voordeel?
- Wie ontwikkelde het eerste algemeen geaccepteerde systeem van biologische classificatie dat hij organismen in twee groepen heeft geclassificeerd?
- Habitatverlies is de grootste bedreiging voor Australische soorten
- Wie is de wetenschapper die zijn primitieve microscoop in 1665 gebruikte om plantmaterialen te observeren, hebben een cellulaire structuur?
- Wat beschrijft het beste een wetenschappelijke theorie?
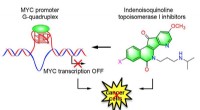
- Nieuwe antikankermiddelen kunnen de tumorgroei bij bijna elk kankertype beter onder controle houden
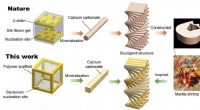
- Kunnen bacteriën sterkere auto's maken, vliegtuigen en bepantsering?
- Video:Waarom hebben we nog geen synthetisch bloed?

- Miniatuur sanitair versnelt de ontwikkeling van medicijnen

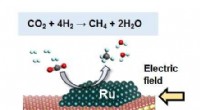
- Nieuwe methode zet koolstofdioxide om in methaan bij lage temperaturen
 Hoe bescherming tegen overstromingen paradoxaal genoeg mensen in gevaar kan brengen
Hoe bescherming tegen overstromingen paradoxaal genoeg mensen in gevaar kan brengen Veranderen hoe we chloor in de bodem bekijken
Veranderen hoe we chloor in de bodem bekijken De 'CES-vloek?' Gadgetshow heeft een slechte reputatie
De 'CES-vloek?' Gadgetshow heeft een slechte reputatie  Sensoren van nanoformaat leveren ongekende gegevens over hoe warmte zich in en uit levende cellen verspreidt
Sensoren van nanoformaat leveren ongekende gegevens over hoe warmte zich in en uit levende cellen verspreidt  Twitteradvocaat zegt dat botgegevens die aan Musk zijn gegeven expliciet een schatting waren
Twitteradvocaat zegt dat botgegevens die aan Musk zijn gegeven expliciet een schatting waren De snelheid van een object omvat?
De snelheid van een object omvat?  Wat is het hoogtenummer van Arizona boven zeeniveau?
Wat is het hoogtenummer van Arizona boven zeeniveau?  Welk stadium zijn chromosomen gedupliceerd?
Welk stadium zijn chromosomen gedupliceerd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


