
Wetenschap
Berylliumverbindingen:reactiviteit en chemische binding
* Beryllium's positie op het periodiek systeem: Beryllium zit in groep 2 (aardalkalimetalen) en heeft een oxidatietoestand van +2. Dit betekent dat het gemakkelijk twee elektronen verliest om een stabiele elektronenconfiguratie te bereiken.
* Vorming van ionische verbindingen: Beryllium vormt gemakkelijk ionische verbindingen met niet-metalen, zoals:
* Zuurstof: BeO (berylliumoxide)
* Chloor: BeCl2 (berylliumchloride)
* Zwavel: BeS (berylliumsulfide)
* Vorming van covalente verbindingen: Beryllium kan ook covalente verbindingen vormen met andere elementen, vooral met halogenen:
* Fluor: BeF2 (berylliumfluoride)
Belangrijke opmerkingen:
* Reactiviteit: Beryllium is een relatief reactief metaal, maar kan worden gestabiliseerd door een beschermende oxidelaag op het oppervlak te vormen.
* Toxiciteit: Berylliumverbindingen zijn giftig en kunnen kankerverwekkend zijn. Dit komt door de kleine omvang van beryllium en het vermogen om gemakkelijk celmembranen te penetreren.
Voorbeelden van veel voorkomende berylliumverbindingen:
* Beryl: Een edelsteen die beryllium, aluminium, silicium en zuurstof (Be3Al2(SiO3)6) bevat.
* Smaragd: Een variëteit van beryl met een groene kleur vanwege chroom- en vanadiumonzuiverheden.
* Aquamarijn: Een verscheidenheid aan beryl met een blauwgroene kleur als gevolg van ijzeronzuiverheden.
Laat het me weten als je meer informatie wilt over specifieke berylliumverbindingen!
 VN doet wereldwijd bod om ongebreidelde vervuiling te beëindigen
VN doet wereldwijd bod om ongebreidelde vervuiling te beëindigen Hoe verklaart de wetenschap het voorkomen van seizoenen op aarde?
Hoe verklaart de wetenschap het voorkomen van seizoenen op aarde?  Invasieve soorten volgen? Volg de mensen
Invasieve soorten volgen? Volg de mensen  Uren om te ontdekken:Onderzoeker onderzoekt hoe de tijd echt aan mensen ontsnapte
Uren om te ontdekken:Onderzoeker onderzoekt hoe de tijd echt aan mensen ontsnapte  Hoe waait de wind van het ene gebied naar het andere?
Hoe waait de wind van het ene gebied naar het andere?
Hoofdlijnen
- Welk type reproductie treedt op wanneer zich een kleine bult of knop vormt op oudercel en vervolgens afbreekt om een nieuwe cel te vormen?
- Wat is reproductieve capaciteit?
- Welk organisme is een herbivoor?
- Waar worden de carriereiwitten en kanaal gevonden?
- Waarom is de studie van cellen belangrijk om levende wezens te begrijpen?
- Sommige bacteriën kunnen zichzelf voortstuwen door vloeistof door middel van een structuur die de?
- Wat is de naam voor een soort die invloed heeft op het overleven van vele andere in uw ecosysteem?
- Welk orgaan staat bekend als chemisch laboratorium in het menselijk lichaam?
- Onderzoekers ontdekken een nieuwe manier om door virussen veroorzaakte kankers te onderdrukken
- Vorming van goudbindingen in realtime gevolgd met behulp van nieuwe moleculaire spectroscopietechniek

- Nieuwe studie vindt onnauwkeurigheden in arseentestkits in Bangladesh

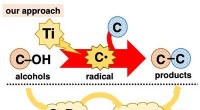
- Alcoholen als voorlopers van koolstofradicaal
- Chemische beeldvorming gebruikt om de diagnose van darmkanker te vergemakkelijken

- Nieuw inzicht brengt duurzame waterstof een stap dichterbij

 Hoe worden natrium en chloor vandaag gebruikt?
Hoe worden natrium en chloor vandaag gebruikt?  Hogere temperatuur, zwaardere regen
Hogere temperatuur, zwaardere regen In welke fase van de materie zijn er deeltjes die niet bewegen?
In welke fase van de materie zijn er deeltjes die niet bewegen?  Waar of onwaar of valse cilia en flagella zijn celoppervlakstructuren die zijn aangepast voor ademhaling?
Waar of onwaar of valse cilia en flagella zijn celoppervlakstructuren die zijn aangepast voor ademhaling?  Zijn sedimentaire rotsen gemaakt van stukken andere rotsen?
Zijn sedimentaire rotsen gemaakt van stukken andere rotsen?  De meeste organismen die in extreme omgevingen leven, zoals warmwater, worden gevonden welk koninkrijk?
De meeste organismen die in extreme omgevingen leven, zoals warmwater, worden gevonden welk koninkrijk?  Hoe worden dierlijke cellen aangepast aan zijn functie?
Hoe worden dierlijke cellen aangepast aan zijn functie?  Wanneer is Redwall kalksteen gevormd?
Wanneer is Redwall kalksteen gevormd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

