
Wetenschap
Moleculaire polariteit begrijpen:VSEPR-theorie en elektronegativiteit
Polariteit begrijpen
* Polariteit komt voort uit een ongelijkmatige verdeling van elektronen in een covalente binding. Dit gebeurt wanneer het ene atoom in de binding een hogere elektronegativiteit heeft (de neiging om elektronen aan te trekken) dan het andere.
* Dipoolmoment: Een molecuul wordt als polair beschouwd als het een netto dipoolmoment heeft, wat betekent dat er een scheiding is tussen positieve en negatieve lading.
* VSEPR (Valence Shell Electron Pair Repulsion) Theorie: Deze theorie helpt bij het voorspellen van de vorm van een molecuul op basis van de rangschikking van elektronenparen rond het centrale atoom.
Factoren die de polariteit beïnvloeden:
* Verschil in elektronegativiteit: Hoe groter het elektronegativiteitsverschil tussen atomen in een binding, hoe polairder de binding.
* Moleculaire geometrie: Zelfs als individuele bindingen polair zijn, kan het molecuul niet-polair zijn als de dipolen van de binding elkaar opheffen vanwege de symmetrische geometrie.
VSEPR-formules en polariteit
Hier leest u hoe VSEPR-formules ons kunnen helpen het meest polaire molecuul te voorspellen:
1. Identificeer moleculen met zeer polaire bindingen: Zoek naar moleculen met grote elektronegativiteitsverschillen tussen het centrale atoom en de omringende atomen. Voorbeelden:
* H-F: Fluor is zeer elektronegatief.
* H-Cl: Chloor is elektronegatief.
* O-H: Zuurstof is elektronegatief.
2. Overweeg moleculaire geometrie:
* Lineair: Lineaire moleculen (AX2) zijn vaak polair als de bindingen polair zijn. Voorbeelden:HF, HCl.
* Gebogen: Gebogen moleculen (AX2E) zijn over het algemeen polair vanwege de ongelijkmatige verdeling van elektronenparen. Voorbeelden:H2O, SO2.
* Trigonaal piramidaal: Trigonale piramidemoleculen (AX3E) zijn polair omdat het centrale atoom omgeven is door drie polaire bindingen en een eenzaam paar. Voorbeeld:NH3.
* Tetraëdrische: Tetraëdrische moleculen (AX4) kunnen polair of niet-polair zijn, afhankelijk van de betrokken atomen. Als alle omringende atomen hetzelfde zijn, kunnen ze niet-polair zijn (bijvoorbeeld CH4). Maar als er verschillende atomen zijn, is het molecuul meestal polair (bijvoorbeeld CHCl3).
Voorbeeld:
* Water (H2O):
* VSEPR-formule:AX2E2 (gebogen)
* Twee H-O-bindingen zijn zeer polair.
* De gebogen geometrie voorkomt dat de bindingsdipolen elkaar opheffen, wat resulteert in een netto dipoolmoment, waardoor het een zeer polair molecuul wordt.
Belangrijke opmerking:
* Hoewel de VSEPR-formules ons een goed uitgangspunt bieden, moet je verwijzen naar elektronegativiteitswaarden en rekening houden met de specifieke betrokken atomen om definitief het meest polaire molecuul te bepalen.
Laat het me weten als je specifieke moleculen in gedachten hebt, en ik kan je helpen hun polariteit te analyseren.
 Fosfor-30 vervalt door positronemissie het product is?
Fosfor-30 vervalt door positronemissie het product is?  Wat nemen chemische veranderingen altijd op of geven ze af?
Wat nemen chemische veranderingen altijd op of geven ze af?  Hoeveel mol koolstof bevinden zich in een diamant met een gewicht van 1200 gram?
Hoeveel mol koolstof bevinden zich in een diamant met een gewicht van 1200 gram?  Verhouding tussen opgeloste stoffen en oplosmiddelen:de concentratie in oplossingen begrijpen
Verhouding tussen opgeloste stoffen en oplosmiddelen:de concentratie in oplossingen begrijpen  Hoe verschilt u koolmonoxide en dioxide?
Hoe verschilt u koolmonoxide en dioxide?
 Boomringen en de uitbarsting van de Laki-vulkaan:klimaat van dichterbij bekeken
Boomringen en de uitbarsting van de Laki-vulkaan:klimaat van dichterbij bekeken Vier andere dingen die ECOSTRESS kan zien
Vier andere dingen die ECOSTRESS kan zien Vanuatu beveelt evacuatie van eiland met rommelende vulkaan
Vanuatu beveelt evacuatie van eiland met rommelende vulkaan Waarom is een nationaal park niet strikt geclassificeerd als een natuurlijk of door de mens gemaakt ecosysteem?
Waarom is een nationaal park niet strikt geclassificeerd als een natuurlijk of door de mens gemaakt ecosysteem?  2000-2010 droogte in Upper Missouri River Basin droogste in 1, 200 jaar
2000-2010 droogte in Upper Missouri River Basin droogste in 1, 200 jaar
Hoofdlijnen
- Noem de externe spijsverteringsklieren geassocieerd met het systeem van mensen?
- Vertegenwoordigt Cell City een plant of een dier uit?
- Wat gebeurt er met een dierlijke cel in een hypotone oplossing?
- Welk deel van de cel is als een receptenboek?
- Hoe technologie een revolutie teweegbrengt in het insectenonderzoek
- Wat is de formule voor productwetgeving in de biologie?
- De vier hoofdcategorieën van grote biologische moleculen?
- Wie staat bekend als de moeder van de microbiologie?
- Is het waar dat wanneer sommige leden van een soort geïsoleerd raken, ze minder snel nieuwe soorten vormen?
- Nieuw onderzoek heeft tot doel de pijnstillende geheimen van dodelijk slakkengif te ontrafelen

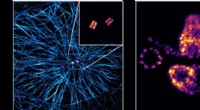
- Vooruitgang in superresolutiemicroscopie
- Wetenschappers kunnen katalysatoren met één atoom voorspellen en ontwerpen voor belangrijke chemische reacties

- Nieuwe stoffen met antivirale eigenschappen

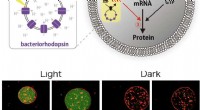
- Wetenschapper bouwt kunstmatige fotosynthetische cellen
 Ben je zoals te wijten aan je genen of omgeving?
Ben je zoals te wijten aan je genen of omgeving?  Wat heeft een afname van de massa voor de frequentie van het systeem?
Wat heeft een afname van de massa voor de frequentie van het systeem?  Heeft een gas zowel de vorm als het volume van zijn container?
Heeft een gas zowel de vorm als het volume van zijn container?  Wat draagt mRNA weg van de kern?
Wat draagt mRNA weg van de kern?  Hoe slaan de meeste planten glucose op?
Hoe slaan de meeste planten glucose op?  Wat betekent semi -behoud in termen van DNA -replicatie?
Wat betekent semi -behoud in termen van DNA -replicatie?  Onderzoekers verlichten het pad naar een nieuw tijdperk van micro-elektronica
Onderzoekers verlichten het pad naar een nieuw tijdperk van micro-elektronica Welke planeten hebben we bezocht?
Welke planeten hebben we bezocht?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

