
Wetenschap
Waterstofbinding is een zwakke aantrekkelijke kracht?
* sterker dan van der Waals Forces: Waterstofbindingen zijn veel sterker dan andere intermoleculaire krachten zoals van der Waals -krachten. Deze sterkte is wat het water mogelijk maakt om vloeistof te zijn bij kamertemperatuur en om DNA zijn dubbele helixstructuur te vormen.
* cruciaal voor biologische systemen: Waterstofbinding speelt een cruciale rol in veel biologische processen. Het houdt DNA -strengen bij elkaar, stabiliseert eiwitstructuren en zorgt ervoor dat water veel moleculen oplost.
Hoewel waterstofbindingen zwakker zijn dan de bindingen die atomen bij elkaar houden in een molecuul, zijn het nog steeds belangrijke krachten die de eigenschappen van veel stoffen beïnvloeden, met name biologische.
 Het potentieel van niet-giftige materialen om lood in perovskietzonnecellen te vervangen
Het potentieel van niet-giftige materialen om lood in perovskietzonnecellen te vervangen Kan fosfor bestaan als covalente kristallen?
Kan fosfor bestaan als covalente kristallen?  Datieve epitaxie:een nieuwe manier om kristalfilms te stapelen
Datieve epitaxie:een nieuwe manier om kristalfilms te stapelen Onderzoekers 3D printen eerste hoogwaardige nanogestructureerde legering die zowel ultrasterk als ductiel is
Onderzoekers 3D printen eerste hoogwaardige nanogestructureerde legering die zowel ultrasterk als ductiel is Welke stap in 6 wetenschappelijke methode zou u de materialen en procedure voor laboratoria vermelden?
Welke stap in 6 wetenschappelijke methode zou u de materialen en procedure voor laboratoria vermelden?
 Voor een CO2-neutraal VK, de komende vijf jaar zijn cruciaal – dit is wat er moet gebeuren
Voor een CO2-neutraal VK, de komende vijf jaar zijn cruciaal – dit is wat er moet gebeuren Delhi-longen worden in dagen ziekelijk bruin
Delhi-longen worden in dagen ziekelijk bruin Biologen identificeren oude stressrespons in koralen
Biologen identificeren oude stressrespons in koralen Wat is kenmerkend voor zowel verwering als erosie?
Wat is kenmerkend voor zowel verwering als erosie?  Aardbevingen gingen door na stopzetting van COVID-19-gerelateerde olie- en gaswinning
Aardbevingen gingen door na stopzetting van COVID-19-gerelateerde olie- en gaswinning
Hoofdlijnen
- Wetenschappers identificeren verborgen genetische variatie die de evolutie helpt stimuleren
- Wat is het vitellinemembraan in een ei?
- Wat is de totale aanvulling van genen in een reproductieve populatie?
- Wat is de kleinste en eenvoudigste ziekte die organismen veroorzaakt?
- Hoe vormen zich nieuwe cellen uit bestaande cellen?
- Wat is de meest gebruikte methode om te klonen?
- Hoe is osmose vergelijkbaar met actief transport?
- Kun je evolueren terwijl je robuust bent?
- Wat zijn de twee orgaansystemen die het meest betrokken zijn bij het produceren van fysiologische veranderingen die leiden tot geschikte gedragspatronen?
- Onderzoekers ontwikkelen nieuw gecombineerd proces voor 3D-printen

- Enigma van vetzuurmetabolisme opgelost - enzymvorm regelt activiteit
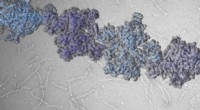
- Onderzoekers beschrijven structuren, mechanismen die bacteriën in staat stellen antibiotica te weerstaan

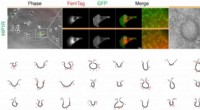
- Nieuwe methode ontdekt om eiwitten in menselijke cellen te bekijken
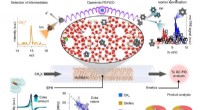
- Reactie-inzichten helpen bij het maken van duurzame vloeibare brandstoffen
 Hoe het buitenaardse handsyndroom werkt
Hoe het buitenaardse handsyndroom werkt  De stijfheid van celplasmamembranen beïnvloedt de opname van nanomedicijnen
De stijfheid van celplasmamembranen beïnvloedt de opname van nanomedicijnen Sealy, 3D-printers van wereldklasse voor het maken van oplosbare medische implantaten
Sealy, 3D-printers van wereldklasse voor het maken van oplosbare medische implantaten Waar komt de blauwgroene kleur van de uranus-sfeer vandaan?
Waar komt de blauwgroene kleur van de uranus-sfeer vandaan?  IJskapstudie belooft nieuwe vooruitzichten voor nauwkeurige lokale klimaatprojecties internationaal
IJskapstudie belooft nieuwe vooruitzichten voor nauwkeurige lokale klimaatprojecties internationaal Waar in het lichaam vindt u de grootste opslag van potentiële energie?
Waar in het lichaam vindt u de grootste opslag van potentiële energie?  Zwakke signalen brengen berichten uit de toekomst
Zwakke signalen brengen berichten uit de toekomst Wilt u vooroordelen op de werkplek elimineren? Let op je beoordelingssysteem, zegt onderzoek
Wilt u vooroordelen op de werkplek elimineren? Let op je beoordelingssysteem, zegt onderzoek
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

